题目内容
11.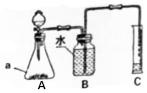 如图为实验室制取并收集一定体积气体(或测量生成气体体积)为分液漏斗图的实验装置图.
如图为实验室制取并收集一定体积气体(或测量生成气体体积)为分液漏斗图的实验装置图.(1)仪器a的名称是锥形瓶.
(2)利用A装置制取气体实验中,检查A装置气密性的方法是关闭分液漏斗的阀门,将导管一端放入水中,用水捂住锥形瓶,一段时间后,若水中的导管口有气泡冒出,手松开,水会倒流进导管口一段距离,则说明气密性良好.
(3)利用该装置制取氧气时,A中发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,若需测量反应生成的氧气体积,装置B中液面上方事先有气泡存在,对测量的结果没有(填“有”或“没有”)影响.
(4)兴趣小组的同学利用该装置测量氢氧化钠的变质程度,方案如下:准确称取一定质量的变质固体样品,放在如图所示装置A中,然后从分液漏斗中加入足量的盐酸,用排水法收集产生的二氧化碳,根据二氧化碳的体积和密度计算变质产物的质量,确定是否完全变质,你认为这个方案不行(填“行”或“不行”),理由是什么?二氧化碳溶于水且与水反应,会导致测量结果偏小.
分析 (1)根据常用仪器的名称分析解答;
(2)根据使用分液漏斗的装置检查气密性方法分析解答;
(3)根据通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气分析解答;
(4)根据二氧化碳能溶于水,不能使用排水法收集进行分析.
解答 解:(1)仪器a的名称是锥形瓶;
故答案为:锥形瓶;
(2)使用分液漏斗的装置检查气密性方法:关闭阀门,将导管一端放入水中,用水捂住锥形瓶,一段时间后,若水中的导管口有气泡冒出,手松开,水会倒流进导管口一段距离,则说明气密性良好;
故答案为:关闭分液漏斗的阀门,将导管一端放入水中,用水捂住锥形瓶,一段时间后,若水中的导管口有气泡冒出,手松开,水会倒流进导管口一段距离,则说明气密性良好;
(3)在实验室用过氧化氢溶液和二氧化锰混合制取氧气不需要加热,可用A装置作为发生装置;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;在测量反应生成的氧气体积时,是利用量筒测量排出水的体积,所以装置B中液面上方事先有气泡存在,对测量的结果不会造成影响;
故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;没有;
(4)这个方案不行,因为CO2能溶于水且与水发生化学反应,造成了二氧化碳的消耗,若用排水法集气,会导致测量的结果偏小;
故答案为:不行;二氧化碳溶于水且与水反应,会导致测量结果偏小
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、检查装置的气密性和反应的类型等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 如图是一瓶刚开启的饮料,其成分中属于有机物的是( )
如图是一瓶刚开启的饮料,其成分中属于有机物的是( )| A. | 只有② | B. | 只有④ | C. | ②④ | D. | ②③④ |
| A. | Na2CO3、NaCl | B. | KCl、Fe(NO3)3 | C. | H2SO4、BaCl2 | D. | KNO3、CuSO4 |
| A. | 将pH试纸湿润后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH | |
| B. | 确定某溶液中是否含有硫酸根离子,可先向该溶液中滴加稀盐酸,若没有任何明显现象,则继续滴加氯化钡溶液,然后观察是否有白色沉淀生成 | |
| C. | 通过灼烧、闻燃烧产生的气味可以鉴别合成纤维与羊毛纤维 | |
| D. | 通过足量灼热的铜网可以除去氮气中混有的少量氧气 |
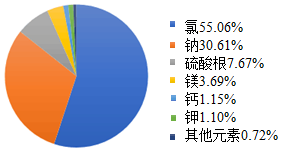 海洋中含有十三亿五千多万立方千米的水,约占地球上总水量的97%.海水是名副其实的液体矿藏,平均每立方公里的海水中有3570万吨的矿物质,世界上已知的100多种元素中,80%可以在海水中找到.如图为海水中溶解的盐分表.海水还是陆地上淡水的来源和气候的调节器,世界海上每年蒸发的淡水有450万立方公里,其中90%通过降雨返回海洋,10%变为雨雪落在大地上,然后顺河流又返回海洋.海水淡化技术正在发展成为产业.有人预计,随着生态环境的恶化,人类解决水荒的最后途径很可能是对海水的淡化.
海洋中含有十三亿五千多万立方千米的水,约占地球上总水量的97%.海水是名副其实的液体矿藏,平均每立方公里的海水中有3570万吨的矿物质,世界上已知的100多种元素中,80%可以在海水中找到.如图为海水中溶解的盐分表.海水还是陆地上淡水的来源和气候的调节器,世界海上每年蒸发的淡水有450万立方公里,其中90%通过降雨返回海洋,10%变为雨雪落在大地上,然后顺河流又返回海洋.海水淡化技术正在发展成为产业.有人预计,随着生态环境的恶化,人类解决水荒的最后途径很可能是对海水的淡化.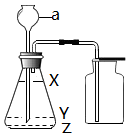 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.