题目内容
4.可乐是一种常见的碳酸饮料,在紧急情况时拧开瓶盖,捂住瓶口使劲摇晃后将喷溅而出的可乐泡沫对准火焰进行喷射就能灭火,下列对可乐及“可乐灭火”分析不正确的是( )| A. | “可乐泡沫”使可燃物隔绝了氧气 | |
| B. | 可乐喷射的水能降低可燃物的着火点 | |
| C. | 上述事实说明碳酸易分解 | |
| D. | 可乐并不是所有火灾都能扑灭 |
分析 根据已有的燃烧的条件和灭火的方法进行分析解答即可.
解答 解:A、“可乐泡沫”使可燃物隔绝了氧气,正确;
B、可燃物的着火点一般不变,错误;
C、捂住瓶口使劲摇晃后将喷溅而出的可乐泡沫对准火焰进行喷射就能灭火,是因为碳酸不稳定,分解成二氧化碳气体,正确;
D、二氧化碳能与活泼的金属镁等反应,因此可乐并不是所有火灾都能扑灭,正确;
故选B.
点评 本题考查的是灭火的原理以及气体溶解度的影响因素,完成此题,可以依据已有的知识进行.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
12.下列关于溶液的说法正确的是( )
| A. | 溶液可以是固体,也可以是液体或气体 | |
| B. | 饱和溶液一定比不饱和溶液所含溶质多 | |
| C. | 长期放置不会分层的液体一定是溶液 | |
| D. | 溶液中只有一种溶质的溶液为纯净物 |
9.在反应X+2Y=R+2M中,已知R和M的相对分子质量之比为4:3,当6gX与Y完全反应后,生成8gR,则反应中Y和M的质量比为( )
| A. | 4:3 | B. | 7:6 | C. | 5:7 | D. | 3:4 |
16.为了测定黄铜(铜、锌合金)中铜的质量分数,取黄铜样品20g加入大烧杯中,把200g稀盐酸分四次加入,实验所得数据如表:
分析表中数据,完成下列问题:
(1)表中m=12.2;
(2)反应总共产生气体的质量为多少?(写出计算过程)
(3)若200g稀盐酸中HCl的质量为14.6g,其余都为水.反应结束后大烧杯中氢元素的质量为21g.
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸的质量/g | 50 | 50 | 50 | 50 |
| 剩余固体的质量/g | 16.75 | 13.5 | m | 12.2 |
(1)表中m=12.2;
(2)反应总共产生气体的质量为多少?(写出计算过程)
(3)若200g稀盐酸中HCl的质量为14.6g,其余都为水.反应结束后大烧杯中氢元素的质量为21g.
14.某金属冶炼厂在生产过程中产生了一定量的含铜废料.化学兴趣小组利用稀硫酸和铁粉分离回收铜,并获得硫酸亚铁晶体.其设计方案如图1所示.
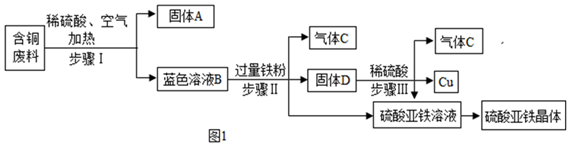
【查阅资料】
①在同温同压下,同体积的气体含有相同的分子数目;
②在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜,反应的化学方程式:2Cu+2H2SO4+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O.
【回答问题】
(1)步骤Ⅰ中分离得到固体A和蓝色溶液B的操作名称是过滤.
(2)蓝色溶液B中的溶质是CuSO4、H2SO4(填化学式).
(3)写出步骤Ⅲ中发生反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(4)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3].根据铜锈的主要成分中含有氢元素和碳元素,可以判断出铜生锈需要空气中的H2O、CO2(填化学式).若要探究“铜生锈是否需要空气中的氧气?”如图2所示实验中,只需完成BD(填字母)两个实验即可达到实验目的.
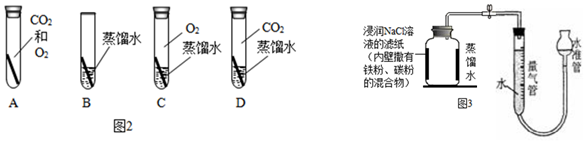
【拓展研究】
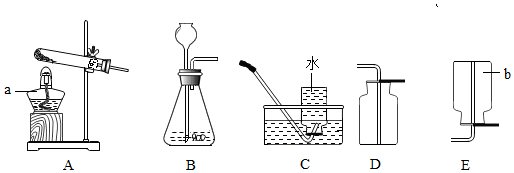
(1)小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图3),9分钟以后测得数据如表:
①请计算出空气中氧气含量20.4%(计算结果保留一位小数).
②炭粉和氯化钠在本实验中的作用是催化作用.
③若将图3装置中的粗铁粉换成足量的铜粉进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由.因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.

【查阅资料】
①在同温同压下,同体积的气体含有相同的分子数目;
②在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜,反应的化学方程式:2Cu+2H2SO4+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O.
【回答问题】
(1)步骤Ⅰ中分离得到固体A和蓝色溶液B的操作名称是过滤.
(2)蓝色溶液B中的溶质是CuSO4、H2SO4(填化学式).
(3)写出步骤Ⅲ中发生反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(4)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3].根据铜锈的主要成分中含有氢元素和碳元素,可以判断出铜生锈需要空气中的H2O、CO2(填化学式).若要探究“铜生锈是否需要空气中的氧气?”如图2所示实验中,只需完成BD(填字母)两个实验即可达到实验目的.

【拓展研究】
(1)小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图3),9分钟以后测得数据如表:
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 量气管内液面所在刻度 | 量气管内液面所在刻度 |
| 150.0mL | 30.8mL | 0.2mL |
②炭粉和氯化钠在本实验中的作用是催化作用.
③若将图3装置中的粗铁粉换成足量的铜粉进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由.因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.
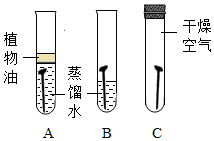 如图所示,取3根粗细、长度均相同的光亮细铁钉,其中两根放入经煮沸迅速冷却的蒸馏水中,A试管上方加一层植物油;C试管中的铁钉放在干燥的空气中,加盖密封.一段时间后观察到:A、C铁钉都没有生锈,而B中铁钉生锈.根据探究回答以下问题:
如图所示,取3根粗细、长度均相同的光亮细铁钉,其中两根放入经煮沸迅速冷却的蒸馏水中,A试管上方加一层植物油;C试管中的铁钉放在干燥的空气中,加盖密封.一段时间后观察到:A、C铁钉都没有生锈,而B中铁钉生锈.根据探究回答以下问题: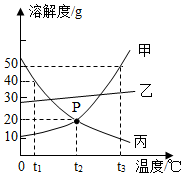 如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线.请根据图回答:
如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线.请根据图回答: