题目内容
3.蚊香是夏日驱除蚊虫的常用物品.丙烯菊酯(化学式:C19H26O3)是蚊香中常含有的高效低毒杀虫剂.(1)丙烯菊酯由三种元素组成,它属于有机物(填物质类别).
(2)点燃蚊香时,要加热使蚊香的温度达到着火点,蚊香才能燃烧.

(3)蚊香在使用过程中(如右图所示),适时熄灭蚊香是节约和安全的需要,请说出熄灭蚊香的一种方法:滴水熄灭.
分析 (1)根据化学式可判断物质的元素组成和物质的种类;
(2)根据燃烧的条件判断;
(3)结合生活实际和灭火的方法解答
解答 解:(1)丙烯菊酯的化学式为C19H26O3由,是由C、H、O 三种元素组成,组成中含有碳元素,属于有机物.
(2)根据燃烧的条件,点燃蚊香时,要加热使蚊香的温度达到着火点,蚊香才能燃烧.
(3)根据灭火的方法和节约的原则,熄灭蚊香可以采用滴水熄灭等方法.
故答案为:(1)有机;
(2)着火点;
(3)滴水熄灭.
点评 此题通过日常生活中的蚊香考查了物质的组成、种类、燃烧的条件和灭火的方法、分子运动等知识,紧密联系生活实际,是一道很好的试题.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
13.下列物质中,不能用来鉴别CO和CO2的是( )
| A. | 澄清的石灰水 | B. | 稀盐酸 | C. | 灼热的氧化铜 | D. | 紫色的石蕊试液 |
11.向稀H2SO4和ZnSO4的混合溶液中,加入一定量的NaOH溶液,充分反应后过滤.在滤液里加入酚酞溶液,无明显变化.下列说法正确的是( )
| A. | 滤液中一定有H2SO4、Na2SO4 | B. | 滤液中一定有Na2SO4、ZnSO4 | ||
| C. | 滤液中可能有H2SO4、ZnSO4 | D. | 滤液中可能有Na2SO4、NaOH |
8.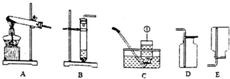 今年的化学实验操作考试有“制取并收集一瓶二氧化碳”的考题.
今年的化学实验操作考试有“制取并收集一瓶二氧化碳”的考题.
(1)实验室制取二氧化碳选用的发生装置和收集装置为BD(填序号),反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究.
【提出问题】:废液中的溶质含有哪些物质
【猜想与假设】:猜想Ⅰ:溶液中的溶质只有CaCl2;
猜想Ⅱ:废液中的溶质有氯化钙和氯化氢.
【进行实验】:兴趣小组的同学取废液进行了以下实验,请你与他们一起完成下列实验报告.
如果猜想Ⅰ正确,有关反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.;
【反思拓展】:如果猜想Ⅱ正确,要使废液中只含有CaCl2,正确的处理方法是加入过量的碳酸钙.
 今年的化学实验操作考试有“制取并收集一瓶二氧化碳”的考题.
今年的化学实验操作考试有“制取并收集一瓶二氧化碳”的考题.(1)实验室制取二氧化碳选用的发生装置和收集装置为BD(填序号),反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究.
【提出问题】:废液中的溶质含有哪些物质
【猜想与假设】:猜想Ⅰ:溶液中的溶质只有CaCl2;
猜想Ⅱ:废液中的溶质有氯化钙和氯化氢.
【进行实验】:兴趣小组的同学取废液进行了以下实验,请你与他们一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的废液于试管中,向其中加入Na2CO3溶液至过量 | 只有沉淀产生 | 猜想Ⅰ正确 |
| 先产生气泡 后产生沉淀 | 猜想Ⅱ正确 |
【反思拓展】:如果猜想Ⅱ正确,要使废液中只含有CaCl2,正确的处理方法是加入过量的碳酸钙.
15.下列生铒中的常见现象,一定包含有化学变化的是( )
| A. | 矿石粉碎 | B. | 铁钉生锈 | C. | 活性炭除臭 | D. | 霓虹灯闪烁 |
12.在下列变化中,属于缓慢氧化的是( )
| A. | 木炭在氧气中燃烧 | B. | 湿衣服晾晒干 | ||
| C. | 食物腐败 | D. | 火药爆炸 |
13.难溶性杂卤石属于“呆矿”,主要成分有K2SO4、MgSO4、CaSO4、不溶性杂质等(假设杂质不参加反应),为能充分利用钾资源,某工厂用溶浸杂卤石制备硫酸钾,工艺流程如下:
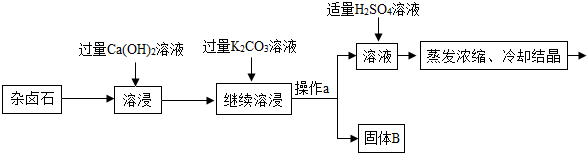
(1)在实验流程中加入过量的Ca(OH)2溶液,目的是出去主要成分中的硫酸镁;发生反应的化学方程式是MgSO4+Ca(OH)2=CaSO4+Mg(OH)2↓.
(2)操作a的名称是过滤.
(3)请写出固体B的两种主要成分Mg(OH)2↓、CaCO3(用化学式表示)
(4)在使用Ca(OH)2溶液和K2CO3溶液对杂卤石进行“溶浸”时,为探究获得较高浸出杂卤石主要成分的浸取率,某实验小组用测得浸取液中K+的质量分数乱来表示浸取率,在相同的时间里,进行了下述实验组:
①上述实验的数据中,温度与K+浸取率的关系是温度越高,浸取率越大.
②上述5组实验中,若要获得最佳的K+浸取率,选择的反应条件是60℃和Ca(OH)23g.

(1)在实验流程中加入过量的Ca(OH)2溶液,目的是出去主要成分中的硫酸镁;发生反应的化学方程式是MgSO4+Ca(OH)2=CaSO4+Mg(OH)2↓.
(2)操作a的名称是过滤.
(3)请写出固体B的两种主要成分Mg(OH)2↓、CaCO3(用化学式表示)
(4)在使用Ca(OH)2溶液和K2CO3溶液对杂卤石进行“溶浸”时,为探究获得较高浸出杂卤石主要成分的浸取率,某实验小组用测得浸取液中K+的质量分数乱来表示浸取率,在相同的时间里,进行了下述实验组:
| 实验 | 温度/℃ | Ca(OH)2用量/g | K+浸取率/% |
| a | 25 | 2.5 | 72.4 |
| b | 40 | 2.5 | 86.55 |
| c | 40 | 3 | 90.02 |
| d | 60 | 3 | 91.98 |
| e | 60 | 4 | 91.45 |
②上述5组实验中,若要获得最佳的K+浸取率,选择的反应条件是60℃和Ca(OH)23g.