题目内容
12.有一包白色粉末,可能由NaCl、Na2SO4、Na2CO3、BaCl2、FeCl3中的一种或几种组成.现做如下试验:①取少量粉末加水溶解,得到无色透明溶液;②另取少量粉末,滴加稀盐酸,有气泡产生.请问:(1)由实验①②可知,原粉末中没有BaCl2FeCl3.(填化学式)
(2)为进一步探究原粉末中的成分,按下图试验:
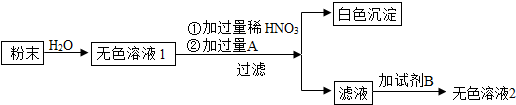
加过量稀HNO3的目的除尽溶液1中的碳酸钠;
加过量A的目的检验并除尽溶液1中的硫酸钠;试剂B为AgNO3;
粉末成分Na2CO3和Na2SO4;无色溶液2中含有的成分NaNO3、AgNO3、HNO3和Ba(NO3)2.
分析 根据氯化铁在溶液中显黄色,碳酸钠和盐酸反应会生成二氧化碳气体,碳酸钠、硫酸钠和氯化钡会生成碳酸钡沉淀、硫酸钡沉淀等知识进行分析.
解答 解:氯化铁在溶液中显黄色,碳酸钠和盐酸反应会生成二氧化碳气体,碳酸钠、硫酸钠和氯化钡会生成碳酸钡沉淀、硫酸钡沉淀.
(1)取少量粉末加水溶解,得到无色透明溶液,氯化铁在溶液中显黄色,所以粉末中不含氯化铁;另取少量粉末,滴加稀盐酸,有气泡产生,碳酸钠和盐酸反应会生成二氧化碳,所以粉末中一定含有碳酸钠,碳酸钠和氯化钡不能共存,粉末中一定不含氯化钡,所以原粉末中没有BaCl2,FeCl3;
(2)检验硫酸钠常用硝酸钡,需要排除碳酸根离子的干扰,碳酸钠和硝酸会生成硝酸钠、水和二氧化碳,所以加入硝酸的目的是:除尽溶液1中的碳酸钠,所以A是硝酸钡,加过量硝酸钡的目的检验并除尽溶液1中的硫酸钠;检验氯离子常用硝酸银,所以试剂B为硝酸银,通过题中的实验现象可知,粉末成分是碳酸钠、硫酸钠,无色溶液2中含有加入的硝酸银,反应剩余的硝酸,硫酸钠和硝酸钡生成的硝酸钠,以及反应剩余的硝酸钡,所以含有的成分为:NaNO3、AgNO3、HNO3和Ba(NO3)2.
故答案为:(1)BaCl2,FeCl3;
(2)除尽溶液1中的碳酸钠,检验并除尽溶液1中的硫酸钠;
AgNO3,Na2CO3和Na2SO4;
NaNO3、AgNO3、HNO3和Ba(NO3)2.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
2.下列实验操作,先后顺序正确的一项是( )
| A. | 检查装置气密性时,先用双手紧贴试管外壁,再将导管的一端浸入水中 | |
| B. | 使用H2O2溶液和MnO2制氧气时,先将药品装入装置,然后检查装置的气密性 | |
| C. | 使用滴管时,先用手指捏紧橡胶乳头,然后把滴管伸入试剂瓶中,放开手指,吸入液体试剂 | |
| D. | 实验室制取、收集氧气时,先将导气管伸入盛满水的集气瓶,再给试管加热 |
3.化学在生活中有广泛的应用,下列说法错误的是( )
| A. | 活性炭可除去水中的异味但不能降低水的硬度 | |
| B. | 使用农药、化肥对人类有利也有弊 | |
| C. | 商家用甲醛溶液浸泡海产品保鲜对顾客有益 | |
| D. | 食用加铁酱油、加碘食盐等可补充人体健康必需的化学元素 |
5.在常温下,不适宜运用物理性质区别的物质组是( )
| A. | 高锰酸钾晶体和氧化铝粉末 | B. | 酒精和食醋 | ||
| C. | 食盐和面粉 | D. | 二氧化锰和木炭粉 |