题目内容
15.由A和B两种元素组成的化合物中,已知A与B的相对原子质量之比为7:2,质量之比为21:8,则该化合物的化学式可能表示为( )| A. | A2B3 | B. | A3B4 | C. | A2B5 | D. | AB |
分析 要确定这种化合物的化学式,必须确定元素A、B在化合物中原子个数关系,可通过假设原子个数的方法,利用所给的数据计算出两元素的原子个数比,最后完成化学式的推断.
解答 解:
设化合物的化学式为AaBb,则元素A的相对原子质量为7M时,元素B的相对原子质量为2M;
化合物AaBb中A、B两元素的质量比=(7M×a):(2M×b)=7a:2b,根据题意:化合物中A、B两元素的质量比为21:8,则
7a:2b=21:8
解得a:b=3:4
则这种化合物的化学式为A3B4;
故选B.
点评 本题考查学生利用化合物中元素的质量比、相对原子质量之比进行推断化学式,考查同学们分析问题、灵活应用所学知识解题的能力.

练习册系列答案
相关题目
3.现有溶质质量分数为8%的食盐水40g,要使溶液中氯化钠的质量分数达到20%,以下说法正确的是( )
| A. | 加入食盐4g | B. | 蒸发水分20g | ||
| C. | 蒸发水分24g | D. | 加入质量分数为25% 的食盐水96g |
4.用试管加热固体时,因操作不正确而出现试管炸裂的现象,其原因可能是( )
| A. | 加热前试管外壁干燥 | |
| B. | 没有预热,加热不均匀,局部温度过高 | |
| C. | 试管口略向下倾斜了 | |
| D. | 试管夹夹在试管中上部了 |
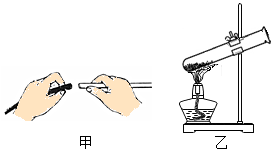 科学实验要注意正确的操作方法,否则会损坏仪器或带来安全威胁.
科学实验要注意正确的操作方法,否则会损坏仪器或带来安全威胁.