题目内容
13.实验表明氯化铁溶液在过氧化氢分解制取氧气的反应中也能起到与二氧化锰相同的作用.某兴趣小组的同学在用42.5g 8%的过氧化氢溶液制取氧气时,向其中加入了4.8g的氯化铁,求:(1)反应结束后,氯化铁的质量为4.8g;
(2)剩余溶液中氯化铁的质量分数.(认为氯化铁全部溶于水,结果保留到0.1%)
分析 由于信息提示“实验表明氯化铁溶液在过氧化氢分解制取氧气的反应中也能起到与二氧化锰相同的作用”,所以过程中氯化铁做催化剂,根据催化剂在反应前后质量不变可推得氯化铁的质量.
由于给出了过氧化氢溶液的质量及其质量分数,所以过氧化氢的质量相当于是已知的.根据过氧化氢的质量和对应的化学方程式可求算生成的氧气的质量,进而求算剩余溶液中氯化铁的质量分数.
解答 解:由于信息提示“实验表明氯化铁溶液在过氧化氢分解制取氧气的反应中也能起到与二氧化锰相同的作用”,所以在该反应中氯化铁做催化剂,而催化剂在反应前后质量不变,所以氯化铁的质量为4.8g
设生成的氧气的质量为x
42.5g 8%的过氧化氢溶液中溶质的质量为42.5g×8%=3.4g
2H2O2$\frac{\underline{\;氯化铁\;}}{\;}$2H2O+O2↑
68 32
3.4g x
$\frac{68}{32}$=$\frac{3.4g}{x}$
x=1.6g
剩余溶液中氯化铁的质量分数为$\frac{4.8g}{42.5g+4.8g-1.6g}$×100%≈10.5%
答:(1)反应结束后,氯化铁的质量为4.8g;
(2)剩余溶液中氯化铁的质量分数约为10.5%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
17.用括号内试剂不能一次性将组内物质鉴别出来的是( )
| A. | 固体:NaOH、NH4NO3、NaCl(水) | |
| B. | 液体:稀盐酸、H2O、Ca(OH)2溶液(石蕊溶液) | |
| C. | 固体:NaCl、CaCO3、KCl(水) | |
| D. | 液体:Ba(NO3)2溶液、MgCl2溶液、K2CO3溶液(稀硫酸) |
4.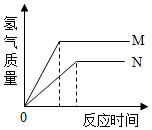 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )| A. | M、N两种金属中较活泼的是N | B. | 生成H2的速率N>M | ||
| C. | 相对原子质量较大的是N | D. | 生成H2的质量M<N |
18.如表图象能正确反映对应变化关系的是( )
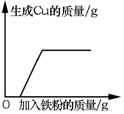 | 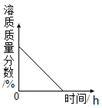 | 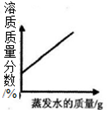 | 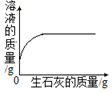 |
| A.向一定质量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉 | B.将浓硫酸露置在空气中 | C.在恒温条件下,将饱和的NaCl溶液蒸发适量水 | D.向一定质量的饱和石灰水中加入生石灰 |
| A. | A | B. | B | C. | C | D. | D |
5.下列鉴别物质的方法错误的是( )
| A. | 用水来鉴别碳酸钙粉末和碳酸钠粉末 | |
| B. | 用酚酞试液鉴别稀盐酸和氯化钠溶液 | |
| C. | 用燃烧的木条鉴别氧气和二氧化碳 | |
| D. | 用熟石灰区别化肥硝酸钾和硝酸铵 |
2.现将一包铜、铝的混合粉末加入到盛有MgCl2、FeCl2溶液的烧杯中,充分反应后溶液呈浅绿色,烧杯中仍有少量固体,关于烧杯中物质组成的说法正确的是( )
| A. | 溶液中溶质为MgCl2、FeCl2,固体为铝和铜 | |
| B. | 溶液中溶质为MgCl2、AlCl3、FeCl2,固体一定含有铝和铜 | |
| C. | 溶液中一定含FeCl2、CuCl2,固体一定含铜 | |
| D. | 溶液中一定含FeCl2,固体一定是铁和铜 |