题目内容
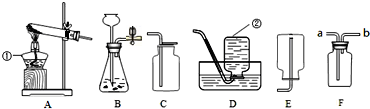
7.如图所示进行实验,测定某赤铁矿样品中氧化铁的质量并回收尾气中的一氧化碳.提示:杂质不参与反应,装置气密性良好,实验前弹簧夹K1、K2均处于关闭状态.

(1)说明装置B的作用及原理.
(2)写出点燃究竟喷灯前应进行的实验操作及意图.
(3)为达到测定目的,需要称量上述实验中哪些物质的质量?如何确定氧化铁的质量?
分析 (1)根据二氧化碳会与氢氧化钠反应生成碳酸钠和水,一氧化碳有毒进行分析;
(2)根据点燃酒精喷灯前应进行的实验操作是检验装置气密性,一氧化碳和空气的混合气点燃可能发生爆炸进行分析;
(3)根据测得实验前、后A装置(包含试管内物质)质量差就是氧化铁中氧元素的质量,然后根据氧化铁中氧元素的质量分数计算得到氧化铁的质量.
解答 解:(1)二氧化碳会与氢氧化钠反应生成碳酸钠和水,一氧化碳有毒,所以B装置的作用是吸收二氧化碳,收集一氧化碳,反应原理是:氢氧化钠和二氧化碳反应生成碳酸钠和水,一氧化碳不会与氢氧化钠反应,密度比液体小;
(2)点燃酒精喷灯前应进行的实验操作是检验装置气密性,一氧化碳和空气的混合气点燃可能发生爆炸;
(3)测得实验前、后A装置(包含试管内物质)质量差就是氧化铁中氧元素的质量,然后依据化学方程式计算得到氧化铁的质量,所以需要称量反应前、后装置A中药品的质量,根据实验前、后A装置(包含试管内物质)质量,可计算二者之差为氧元素的质量,根据氧化铁中氧元素的质量分数,则可求氧化铁的质量.
故答案为:(1)吸收二氧化碳,收集一氧化碳;氢氧化钠和二氧化碳反应生成碳酸钠和水,一氧化碳不会与氢氧化钠反应,密度比液体小;
(2)检验装置气密性,一氧化碳和空气的混合气点燃可能发生爆炸;
(3)反应前、后装置A中药品的质量,根据实验前、后A装置(包含试管内物质)质量差,可计算二者之差为氧元素的质量,根据氧化铁中氧元素的质量分数,则可求氧化铁的质量.
点评 运用对一氧化碳还原氧化铁反应操作的理解,推断各装置的作用,并能进行简单的分析,是解答类似问题的一般方法.

练习册系列答案
相关题目
17.如表是某同学探究金属活动性顺序的实验报告,请你在空白处填空.
| 实验步骤 | 实验现象 | 解释 |
| (1)将铁片、铜片分别投入到盛有稀盐酸的试管中. | 铁片的表面产生大量的气泡;铜片表面无现象; | 反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑ |
| (2)将铜片投入到盛有AgNO3溶液的试管中. | 在铜片的表面覆盖了一层银白色物质,溶液呈蓝色. | 反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 结论:Fe、Cu、Ag三种金属由强到弱的活动顺序为:Fe>Cu>Ag. | ||
2.“庄稼一枝花,全靠肥当家”.下列关于农作物和化肥、农药说法正确的是( )
| A. | (NH4)2SO4属于复合肥料 | |
| B. | NH4Cl 与熟石灰混合施用可以提高肥效 | |
| C. | 硫酸钾和草木灰(K2CO3)均可用作钾肥 | |
| D. | 农作物所必需营养元素只有氮、磷和钾三种 |
19.以下生产、生活中的做法不符合环保理念的是( )
| A. | 秸杆回收利用,不露天焚烧 | |
| B. | 购物时用布袋、纸袋等代替塑料袋 | |
| C. | 减少使用一次性木筷 | |
| D. | 废旧电池回收利用将价值不大,随意丢弃 |
17.程浩同学查阅资料得知:Cu与稀硫酸不反应,但Cu可与浓硫酸在加热的条件下反应,化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2R,下列说法中不正确的是( )
| A. | 该反应中涉及了3种类型的化合物 | |
| B. | R为相对分子质量最小的氧化物 | |
| C. | 反应前后,H2SO4中硫的化合价全部发生了改变 | |
| D. | 该反应不属于四种基本反应类型中的任何一种 |
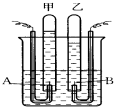 如图是实验室电解水的简易装置示意图.
如图是实验室电解水的简易装置示意图.