题目内容
14.化学小组在用锌粒和硫酸溶液反应制取氢气时,发现生成的气体有刺激性气味,于是对反应中气体的成分进行了如下探究.请你参与他们的探究,并回答有关问题:【提出猜想】
小明认为锌粒和硫酸溶液反应有氢气产生,因为锌位于金属活动性顺序中H的前面.
小红认为可能还有二氧化硫产生,她的理由是:①二氧化硫是一种刺激性气味的气体;②硫酸溶液中含有硫元素.
【查阅资料】二氧化硫与二氧化碳具有相似的化学性质.
【实验方案】小组同学设计了如图所示装置进行实验,并用三种浓度的硫酸进行了实验.
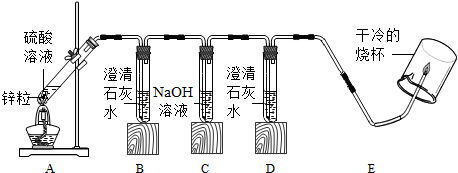
(1)若气体中含有二氧化硫,装置B中应出现CaSO3白色沉淀.则二氧化硫与石灰水反应的化学方程式为SO2+Ca(OH)2=CaSO3↓+H2O.
(2)装置C中NaOH溶液的作用是充分吸收二氧化硫.
(3)为检验气体中是否含有氢气,需在装置E的尖嘴导管处点燃气体,并将干冷的烧杯倒扣在尖嘴导管的上方.若观察到气体可以燃烧,且烧杯内壁有水雾,说明气体中含有氢气.为保证实验安全,在点燃气体前,必须进行的实验操作是验纯.
(4)实验中实际观察的现象如下:
| A中硫酸的 质量分数 | 实验现象 | |||
| B中 | D中 | E处 | ||
| 实验一 | 98% | 变浑浊 | 不变浑浊 | 不可燃 |
| 实验二 | 50% | 稍变浑浊 | 不变浑浊 | 可燃 |
| 实验三 | 25% | 不变浑浊 | 不变浑浊 | 可燃 |

【交流反思】根据本次探究的结果和所学知识分析,可能会对化学反应中产物的种类产生影响的是AC(填序号).
A.反应物的质量比 B.反应物的接触面积 C.反应物的浓度大小.
分析 【提出猜想】根据质量守恒定律,化学反应前后元素的质量和种类不变解答;
【实验方案】
(1)根据二氧化硫与石灰水反应的原理,写出反应的化学方程式解答、
(2)根据氢氧化钠溶液能够吸收二氧化硫,并且氢氧化钠和二氧化硫反应生成亚硫酸钠和水解答;
(3)根据氢气燃烧生成水;氢气点燃时易发生爆炸解答;
(4)根据质量守恒定律,化学反应前后原子的个数和种类不变解答;
【交流反思】根据实验中实际观察的现象进行分析解答.
解答 解:
【提出猜想】根据质量守恒定律,化学反应前后元素的质量和种类不变,锌粒和硫酸溶液反应还有二氧化硫产生,理由是:①二氧化硫是一种刺激性气味的气体;②硫酸溶液中含有硫元素;
【实验方案】
(1)二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,反应的化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O.
(2)氢氧化钠溶液能够吸收二氧化硫,故实验C装置的作用是吸收二氧化硫;
(3)为检验气体中是否含有氢气,需在装置E的尖嘴导管处点燃气体,并将干冷的烧杯倒扣在尖嘴导管的上方.若观察到气体可以燃烧,且烧杯内壁有水雾,说明气体中含有氢气.为保证实验安全,在点燃气体前,必须进行的实验操作是验纯;
(4)根据质量守恒定律,化学反应前后原子的个数和种类不变,反应前Zn、S、O、H原子个数分别是1、2、8、4;反应后Zn、S、O、H原子个数分别是1、1、6、4;锌与浓度较大的硫酸生二氧化硫的化学方程式为:Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O;
【交流反思】根据本次探究的结果和所学知识分析,可能会对化学反应中产物的种类产生影响的是反应物的质量比、反应物的浓度大小.
答案:
【提出猜想】②硫酸溶液中含有硫元素;
【实验方案】(1)SO2+Ca(OH)2=CaSO3↓+H2O.
(2)充分吸收二氧化硫;
(3)烧杯内壁有水雾; 验纯;
【实验结论】Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O;
【交流反思】AC
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 阅读快车系列答案
阅读快车系列答案| A | B | C | D |
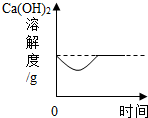 |  | 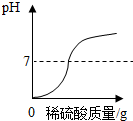 | 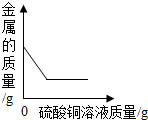 |
| 向饱和石灰水中加入一定量CaO | 一定温度下,向不饱和和硝酸钾溶液中加入硝酸钾固体 | 向一定量NaOH溶液中加稀H2SO4 | 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
| A. | Ca(H2PO4)2 | B. | NH4NO3 | C. | K2SO4 | D. | NH4H2PO4 |
 (1)海沙是由石英和贝壳的碎片组成,石英的主要成分是(用化学符号表示,下同)SiO2,贝壳的主要成分是CaCO3;
(1)海沙是由石英和贝壳的碎片组成,石英的主要成分是(用化学符号表示,下同)SiO2,贝壳的主要成分是CaCO3;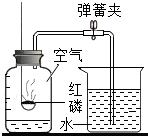 如图所示进行空气中氧气含量测定实验,用微粒观点解释以下实验现象.
如图所示进行空气中氧气含量测定实验,用微粒观点解释以下实验现象.