题目内容
金属在生产生活中应用广泛.
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
(2)铁生锈的条件是 ,将生锈的铁片放在硫酸和硫酸铜的混合溶液中,可能发生的复分解反应的化学方程式是
(3)金属的回收和利用是保护金属资源的一种有效途径.
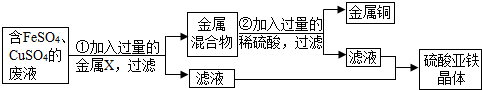
①将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是
A.肯定有银 B.肯定有铜 C.可能有铁 D.可能是铁和银
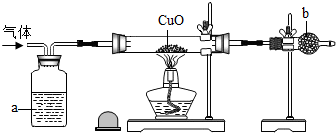
②废钢铁可回收重新冶炼,如图所示是用一氧化碳还原氧化铁的简易装置:此实验中现象为 ,发生反应的化学方程式为 .该装置没有对尾气进行处理会污染空气,为使实验更加环保,你认为可行的改进方法是 
(4)用不纯的锌与稀硫酸反应能加快产生氢气的速率,实验室用13g锌粉和2g铜粉的混合物与足量的稀硫酸反应,可生成多少克氢气?
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
(2)铁生锈的条件是
(3)金属的回收和利用是保护金属资源的一种有效途径.
①将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是
A.肯定有银 B.肯定有铜 C.可能有铁 D.可能是铁和银
②废钢铁可回收重新冶炼,如图所示是用一氧化碳还原氧化铁的简易装置:此实验中现象为

(4)用不纯的锌与稀硫酸反应能加快产生氢气的速率,实验室用13g锌粉和2g铜粉的混合物与足量的稀硫酸反应,可生成多少克氢气?
考点:金属锈蚀的条件及其防护,金属的化学性质,一氧化碳还原氧化铁,地壳中元素的分布与含量,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:金属与金属材料
分析:(1)铝元素是地壳中含量最多的金属元素;
(2)铁和水、氧气同时接触时容易生锈;
氧化铁和稀硫酸反应生成硫酸铁和水,铁和稀硫酸反应生成硫酸亚铁和氢气,铁和硫酸铜反应生成硫酸亚铁和铜;
(3)将铁粉和铜粉的混合物放入硝酸银溶液中,铁先和硝酸银反应,铁完全反应后,如果硝酸银有剩余,铜再和硝酸银反应;
氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳;
一氧化碳有毒,逸散到空气中会污染环境;
(4)根据锌的质量可以计算反应生成氢气的质量.
(2)铁和水、氧气同时接触时容易生锈;
氧化铁和稀硫酸反应生成硫酸铁和水,铁和稀硫酸反应生成硫酸亚铁和氢气,铁和硫酸铜反应生成硫酸亚铁和铜;
(3)将铁粉和铜粉的混合物放入硝酸银溶液中,铁先和硝酸银反应,铁完全反应后,如果硝酸银有剩余,铜再和硝酸银反应;
氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳;
一氧化碳有毒,逸散到空气中会污染环境;
(4)根据锌的质量可以计算反应生成氢气的质量.
解答:解:(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是铝元素.
故填:铝.
(2)铁生锈的条件是与水和氧气同时接触,将生锈的铁片放在硫酸和硫酸铜的混合溶液中,可能发生的复分解反应的化学方程式是:
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故填:与水和氧气同时接触;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(3)①A.肯定有银,这是因为首先反应的是硝酸银和铁,即只要反应既能够生成银,该选项说法正确;
B.不一定有铜,如果硝酸银过量,则剩余固体中不含有铜,该选项说法不正确;
C.如果铁过量,剩余固体中含有铁,该选项说法正确;
D.不可能是铁和银,因为如果含有铁和银,则一定含有铜,该选项说法不正确.
故填:AC.
②此实验中现象为红色粉末逐渐变成黑色,发生反应的化学方程式为:Fe2O3+3CO
2Fe+3CO2;
为使实验更加环保,你认为可行的改进方法是用塑料袋把一氧化碳收集起来.
故填:红色粉末逐渐变成黑色;Fe2O3+3CO
2Fe+3CO2;用塑料袋把一氧化碳收集起来.
(4)设生成氢气的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
13g x
=
,
x=0.4g,
答:生成氢气的质量是0.4g.
故填:铝.
(2)铁生锈的条件是与水和氧气同时接触,将生锈的铁片放在硫酸和硫酸铜的混合溶液中,可能发生的复分解反应的化学方程式是:
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故填:与水和氧气同时接触;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(3)①A.肯定有银,这是因为首先反应的是硝酸银和铁,即只要反应既能够生成银,该选项说法正确;
B.不一定有铜,如果硝酸银过量,则剩余固体中不含有铜,该选项说法不正确;
C.如果铁过量,剩余固体中含有铁,该选项说法正确;
D.不可能是铁和银,因为如果含有铁和银,则一定含有铜,该选项说法不正确.
故填:AC.
②此实验中现象为红色粉末逐渐变成黑色,发生反应的化学方程式为:Fe2O3+3CO
| ||
为使实验更加环保,你认为可行的改进方法是用塑料袋把一氧化碳收集起来.
故填:红色粉末逐渐变成黑色;Fe2O3+3CO
| ||
(4)设生成氢气的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
13g x
| 65 |
| 13g |
| 2 |
| x |
x=0.4g,
答:生成氢气的质量是0.4g.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学用语正确的是( )
| A、一个一氧化碳分子:Co |
| B、2个水分子:2H2O2 |
| C、3个钠离子:3Na+ |
| D、4个氢原子:2H2 |
向水中加入下列物质,水的温度明显下降的是( )
| A、CaO |
| B、NaOH |
| C、浓硫酸 |
| D、NH4NO3 |