题目内容
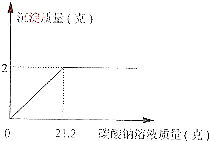 (2009?湘西州)一盐场生产的食盐产品中含有氯化钙杂质,为测定该食盐产品中氯化钠的质量分数,某校化学兴趣小组进行了如下实验:取100g食盐样品完全溶解于水,逐滴加入碳酸钠溶液,反应关系如下图所示,试计算:
(2009?湘西州)一盐场生产的食盐产品中含有氯化钙杂质,为测定该食盐产品中氯化钠的质量分数,某校化学兴趣小组进行了如下实验:取100g食盐样品完全溶解于水,逐滴加入碳酸钠溶液,反应关系如下图所示,试计算:(相对原子质量:C-12、O-16、Cl-35.5、Na-23、Ca-40)
(1)该食盐产品的氯化钠质量分数?
(2)滴加碳酸钠溶液的溶质质量分数?
分析:根据图可知,加碳酸钠溶液21.2g时完全反应,共生成沉淀2g,将2g碳酸钙的质量代入化学反应方程式可计算氯化钙的质量及碳酸钠的质量,再计算质量分数.
解答:解:设100g食盐样品中氯化钙的质量为x,消耗的碳酸钠的质量为y,
则CaCl2+Na2CO3═CaCO3↓+2NaCl
111 106 100
x y 2g
=
,
=
,
解得x=2.22g,y=2.12g,
(1)100g食盐样品中氯化钠的质量为100g-2.22g=97.78g,
则该食盐产品的氯化钠质量分数为
×100%=97.78%,
答:该食盐产品的氯化钠质量分数为97.78%;
(2)由图可知碳酸钠溶液的质量为21.2g,
则碳酸钠溶液的溶质质量分数为
×100%=10%,
答:碳酸钠溶液的溶质质量分数为10%.
则CaCl2+Na2CO3═CaCO3↓+2NaCl
111 106 100
x y 2g
| 111 |
| x |
| 100 |
| 2g |
| 106 |
| y |
| 100 |
| 2g |
解得x=2.22g,y=2.12g,
(1)100g食盐样品中氯化钠的质量为100g-2.22g=97.78g,
则该食盐产品的氯化钠质量分数为
| 97.78g |
| 100g |
答:该食盐产品的氯化钠质量分数为97.78%;
(2)由图可知碳酸钠溶液的质量为21.2g,
则碳酸钠溶液的溶质质量分数为
| 2.12g |
| 21.2g |
答:碳酸钠溶液的溶质质量分数为10%.
点评:本题考查化学反应及图象相结合的计算,明确图中的线、点、面的意义,利用沉淀的质量代入化学反应方程式计算是解答的关键.

练习册系列答案
相关题目
