题目内容
10.氨基钠(NaNH2)是生产维生素A的原料.工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至一定温度生成氨基钠和氢气.下列说法不正确的是( )| A. | NaNH2中氮元素的化合价为-3价 | |
| B. | NaNH2中钠元素的质量分数为35.9% | |
| C. | 钠的熔点比铁的熔点低 | |
| D. | 该反应的化学方程式为:4Na+4NH3$\frac{\underline{\;\;△\;\;}}{\;}$4NaNH2+H2↑ |
分析 A、根据在化合物中正负化合价代数和为零,进行分析判断.
B、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析判断.
C、根据金属钠于97~100℃熔融,进行分析判断.
D、根据题意,将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至一定温度生成氨基钠和氢气,进行分析判断.
解答 解:A、氢、钠元素均显+1价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(+1)×2=0,则x=-3价,故选项说法正确.
B、NaNH2中钠元素的质量分数为$\frac{23}{23+14+1×2}$×100%≈58.9%,故选项说法错误.
C、金属钠于97~100℃熔融,说明其熔点小于97~100℃,而铁的熔点较高,钠的熔点比铁的熔点低,故选项说法正确.
D、将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至一定温度生成氨基钠和氢气,反应的化学方程式为2Na+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNH2+H2,选项中化学方程式配平错误,反应物中氨气是气体,氢气的后面不需要标注↑,故选项说法错误.
故选:BD.
点评 本题难度不大,理解制取氨基钠的反应原理,掌握化合价的原则、化学式的有关计算等是正确解答本题的关键.

练习册系列答案
相关题目
18.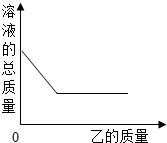 向一定质量的甲中连续加入乙至过量,此过程中溶液的总质量与加入乙的质量之间关系,符合如图曲线表示的是( )
向一定质量的甲中连续加入乙至过量,此过程中溶液的总质量与加入乙的质量之间关系,符合如图曲线表示的是( )
 向一定质量的甲中连续加入乙至过量,此过程中溶液的总质量与加入乙的质量之间关系,符合如图曲线表示的是( )
向一定质量的甲中连续加入乙至过量,此过程中溶液的总质量与加入乙的质量之间关系,符合如图曲线表示的是( )| 甲 | 乙 | |
| A | 稀硫酸 | 氢氧化钠溶液 |
| B | 稀盐酸 | 碳酸钙粉末 |
| C | 稀盐酸 | 锌粒 |
| D | 硝酸银溶液 | 铜粉 |
| A. | A | B. | B | C. | C | D. | D |
15.下列物质化学式书写正确的是( )
| A. | 铝:AL | B. | 氯化钾:KCl2 | ||
| C. | 硫酸铜:CuSO4 | D. | 四氧化三铁:O4Fe3 |
2.下列关于氧气的说法正确的是( )
| A. | 液态氧可用作火箭的助燃剂 | |
| B. | 氧气在空气中的体积分数为78% | |
| C. | 硫在氧气中燃烧发出黄色火焰 | |
| D. | 鱼类能在水中生存,证明氧气易溶于水 |
20. 如图为两种物质间发生化学反应的微观示意图(一种小球代表一种原子).下列说法中正确的是( )
如图为两种物质间发生化学反应的微观示意图(一种小球代表一种原子).下列说法中正确的是( )
 如图为两种物质间发生化学反应的微观示意图(一种小球代表一种原子).下列说法中正确的是( )
如图为两种物质间发生化学反应的微观示意图(一种小球代表一种原子).下列说法中正确的是( )| A. | 图示中共有三种单质分子 | |
| B. | 图示产物为混合物 | |
| C. | 图示说明在化学反应中分子不可再分 | |
| D. | 图示化学反应属于化合反应 |
 2016年3月22日是第二十四届“世界水日”,今年的宣传主题是“水与就业”,请回答下列问题:
2016年3月22日是第二十四届“世界水日”,今年的宣传主题是“水与就业”,请回答下列问题:
