题目内容
化学语言包括文字语言、符号语言、图表语言等.
(1)用文字描述下列化学符号的意义:
①2H2O2 ②O
③5Si ④3Ca2+
(2)用下列字母序号填空:
a.Mg b.N2 c.O2 d.CO
① 用于急救病人
② 可充入食品包装
③ 可制作照明弹
④ 是管道煤气的主要成分
(3)写出下列反应的化学方程式:
①红磷在空气中燃烧 .
②铜绿受热分解 .
③铁和硫酸铜溶液 .
④硝酸铵受热分解生成N2O气体和水 .
| 化学符号及其周围数字的意义;常见气体的用途;金属的物理性质及用途;书写化学方程式、文字表达式、电离方程式.. | |
| 专题: | 物质的性质与用途;化学用语和质量守恒定律. |
| 分析: | 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目. |
| 解答: | 解:(1))①化学式前面的数字表示分子的个数,故2H2O2表示2个过氧化氢分子; ②根据元素符号的意义可知,O可表示氧元素或一个氧原子; ③元素符号前面的数字表示原子的个数,故5Si表示5个硅原子; ④离子符号前面标上数字表示几个这样的离子,故3Ca2+表示3个钙离子; (2)①氧气能供给呼吸,常用于急救病人; ②氮气化学性质稳定,可作为保护气充入食品包装; ③金属镁在燃烧时发出耀眼的白光,常做照明弹; ④一氧化碳具有可燃性,是管道煤气的主要成分; (3)①红磷在空气中燃烧生成五氧化二磷,反应的化学方程式为4P+5O2 ②铜绿受热分解,已知此反应的反应物、生成物、反应条件,则可知其化学方程式为:Cu2(OH)2CO3 ③铁和硫酸铜溶液反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu; ④硝酸铵受热分解生成N2O气体和水,反应的化学方程式为NH4NO3 故答案为: (1)①2个过氧化氢分子 ②氧元素或一个氧原子 ③5个硅原子 ④3个钙离子 (2)①c ②b ③a ④d (3)①4P+5O2 ②Cu2(OH)2CO3 ③Fe+CuSO4=FeSO4+Cu ④NH4NO3 |
| 点评: | 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易. |

在讨论天然气的主要成分CH4的意义时,下列四位同学中哪个说法是错误的( )
|
| A. | B. | C. | D. |
某无色气体可能由H2、CH4、CO、CO2中的几种组成。将些混合气体通过足量的澄清石灰水,出现白色浑浊;将剩余气体导出,经干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成。该混合气体的组成不可能是( )
A.H2、CH4、CO B.H2、 CO2 C.CH4 、CO2 D.CH4、CO、H2、CO2w
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | CO | 将气体点燃 |
| B | N2 | O2 | 通过灼热的铜网 |
| C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | FeCl2 | CuCl2 | 加入过量的铁粉,过滤 |
下列属于置换反应的是( )
|
| A. | 制漂白粉 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O |
|
| B. | 高炉炼铁 3CO+Fe2O3 |
|
| C. | 潜艇供氧 2Na2O2+2H2O═4NaOH+O2↑ |
|
| D. | 焊接铁轨 2Al+Fe2O3 |
据中央电视台6月3日对云南抚仙湖底古城考古的现场报道,科学家曾经通过测定古生物遗骸中的碳﹣14来推断古城年代.碳﹣14原子的核电荷数为6,质子数和中子数之和为14,下列关于碳﹣14原子的说法中错误的是( )
|
| A. | 质子数为6 | B. | 中子数为6 |
|
| C. | 电子数为6 | D. | 电子数和中子数之和为14 |
下列事实不能说明分子之间有间隔的是( )
|
| A. | 打气筒将空气压入自行车胎内 |
|
| B. | 空气受热体积膨胀 |
|
| C. | 氢气在氧气中燃烧生成水 |
|
| D. | 1体积酒精和1体积水混合小于2体积 |
化学用语是我们学习化学的重要工具。下图为七种原子的结构示意图,请按要求填空。
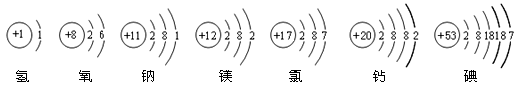 |
(1)上图中七种元素之间的最本质的区别是 ;
(2)钠原子在化学反应中容易 (选填“得到”或“失去”)电子,它与氯形成的化合物的化学式为 ;这种化合物的构成粒子是 ;(填粒子符号)
(3)从原子结构上分析,图中哪两组元素具有相似化学性质 ; (填元素符号)
(4)氧化钙常用作干燥剂,该干燥剂与水反应会 (选填“吸热”或“放热”);
(5)碘元素是人体必需的微量元素,它处于元素周期表中的第 周期。
 2P2O5;
2P2O5; 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O  2P2O5
2P2O5 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑ 2Fe+3CO2
2Fe+3CO2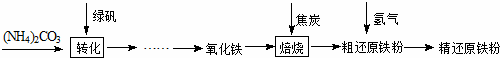
 xFe+yH2O Fe3C+2H2
xFe+yH2O Fe3C+2H2 3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .
3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .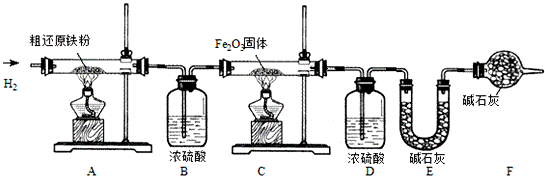
 3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).