题目内容
1.化学兴趣小组同学发现实验台上按如图所示顺序摆放着6瓶不同的无色溶液(如图所示:A、B、C、D、E、F代表对应的溶液).其中E溶液的试剂瓶标签破损.为此,他们做了如下探究:
【提出问题】E溶液的成分是什么?
【提出猜想】Ⅰ:NaOH溶液;Ⅱ:Na2CO3溶液;Ⅲ:Na2SO4溶液;Ⅳ:NaCl溶液
【验证猜想】按如下步骤进行
| 步骤一 | 步骤二 | 步骤三 |
 |  |  |
①实验一如出现红色,李成同学即认为“猜想Ⅰ”正确,张平同学认为“猜想Ⅰ”不一定正确,他的理由是碳酸钠溶液也显碱性,同时他认为可省去实验二(或三)( 填“一”或“二”或“三”)就可得出结论.如E溶液是NaOH溶液,则依据的实验现象是加入足量盐酸没有气泡产生.
②实验一如没有出现红色,也再需一步实验即可得出结论,该步实验滴加的试剂是BaCl2,如发生化学反应,写出发生反应的化学方程式BaCl2+Na2SO4=2NaCl+BaSO4↓.
【反思与评价】
D、E试剂瓶需要密封保存的原因是氢氧化钠和氢氧化钙溶液容易吸收空气中的二氧化碳.
分析 根据已有的知识进行分析解答,氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,碳酸钠溶液呈碱性,能使酚酞试液变红,能与盐酸反应产生二氧化碳气体;据此解答.
解答 解:分析与推理:①碳酸钠的水溶液呈碱性,能使酚酞试液变红,故出现红色不一定是氢氧化钠溶液;可以省略实验二或三,氢氧化钠溶液与盐酸混合没有明显的现象,故填:碳酸钠溶液也显碱性,二(或三),加入足量盐酸没有气泡产生;
②实验一如没有出现红色,说明溶液不呈碱性,需要加入氯化钡溶液检验是否是硫酸钠溶液,氯化钡能与硫酸钠反应产生硫酸钡沉淀,故填:BaCl2,BaCl2+Na2SO4=2NaCl+BaSO4↓;
反思与评价:氢氧化钠和氢氧化钙溶液容易吸收空气中的二氧化碳,故需要密封保存,故填:氢氧化钠和氢氧化钙溶液容易吸收空气中的二氧化碳.
点评 本题是缺失标签的实验探究题,相当于物质鉴别题,在鉴别几种物质时要从物质的不同性质入手,但试题涉及知识点多,要加强知识的全面性和系统性.特别注意检验溶液是否是氢氧化钠溶液,就需要排除碳酸钠对氢氧化钠的鉴定干扰,加入足量的氯化钙溶液可使碳酸根转化成沉淀,而后对溶液用酚酞试液进行检验,只要溶液此时变红,则可证明氢氧化钠的存在.

练习册系列答案
相关题目
11.下列实验操作正确的是( )
| A. | 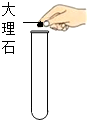 取固体药品 | B. |  稀释浓硫酸 | C. | 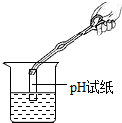 测液体pH | D. | 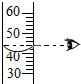 读液体体积 |
12.根据所学化学知识,判断下列说法中完全正确的是( )
| A. | 硫酸铵与熟石灰混合施用,不但能增加肥效,还可以改良酸性土壤 | |
| B. | 除去一氧化碳中混有的二氧化碳可通过灼热的氧化铜 | |
| C. | 物质与氧发生的反应属于氧化反应,氧气具有氧化性 | |
| D. | 燃烧都是剧烈的发热发光的化合反应 |
16.松花蛋,又称皮蛋.其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.请回答下列问题:
(1)静置后,取少量的上层料液,稀释后滴加无色酚酞试液.则无色酚酞试液变为红色.
(2)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaCl和NaOH,
②可能还含有其它溶质:
甲同学推断只有Ca(OH)2
乙同学推断只有Na2CO3
丙同学推断有Ca(OH)2 也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
【探究结论】同学甲的推断是正确的.
【知识应用】皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是酸碱中和.
(1)静置后,取少量的上层料液,稀释后滴加无色酚酞试液.则无色酚酞试液变为红色.
(2)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaCl和NaOH,
②可能还含有其它溶质:
甲同学推断只有Ca(OH)2
乙同学推断只有Na2CO3
丙同学推断有Ca(OH)2 也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
【知识应用】皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是酸碱中和.
5.氧气是人类生产活动的重要资源,关于氧气的性质及用途说法错误的是( )
| A. | 具有可燃性 | B. | 具有氧化性 | C. | 可供动植物呼吸 | D. | 不易溶于水 |
10.用一种试剂一次就可鉴别Na2SO4、Ca(OH)2、稀HCl三种溶液,该试剂是( )
| A. | 酚酞试液 | B. | 硝酸钡溶液 | C. | 碳酸钠溶液 | D. | 氢氧化钡溶液 |
 A、B、C三种物质的溶解度曲线如图所示,回答下列问题:
A、B、C三种物质的溶解度曲线如图所示,回答下列问题: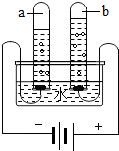 2013年张家界市初中毕业化学实验操作技能考查中,小波抽到的试题是“水的净化”,请你与小波一起实验,并回答下列问题.
2013年张家界市初中毕业化学实验操作技能考查中,小波抽到的试题是“水的净化”,请你与小波一起实验,并回答下列问题.