题目内容
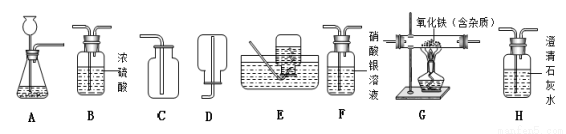
(7分)根据下图回答问题。
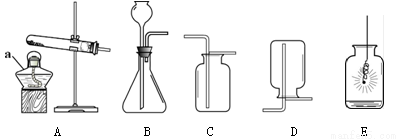
(1)仪器a的名称是 。
(2)实验室用高锰酸钾制取氧气的化学方程式为,选用的收集装置是(填字母序号,下同)。如图E所示,铁丝与氧气反应的化学方程式为 。
(3)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为 ,选用的发生装置是 。将燃着的木条放在瓶口,若观察到 ,说明瓶中已充满二氧化碳。
(1)酒精灯(2)2KMnO4 K2MnO4+MnO2+O2↑C3Fe+2O2
K2MnO4+MnO2+O2↑C3Fe+2O2 Fe3O4(3)CaCO3+2HCl===CaCl2+H2O+CO2↑B木条熄灭
Fe3O4(3)CaCO3+2HCl===CaCl2+H2O+CO2↑B木条熄灭
【解析】
试题分析:根据所学知识可知,(1)仪器a的名称是酒精灯;(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4 K2MnO4+MnO2+O2↑,因为固体加热制取密度比空气大的氧气,故气体收集装置选择C,铁丝与氧气反应的化学方程式为3Fe+2O2
K2MnO4+MnO2+O2↑,因为固体加热制取密度比空气大的氧气,故气体收集装置选择C,铁丝与氧气反应的化学方程式为3Fe+2O2 Fe3O4(3)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为CaCO3+2HCl===CaCl2+H2O+CO2↑,因为固液常温下反应,故选用的发生装置是B,将燃着的木条放在瓶口,若观察到木条熄灭,说明瓶中已充满二氧化碳。
Fe3O4(3)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为CaCO3+2HCl===CaCl2+H2O+CO2↑,因为固液常温下反应,故选用的发生装置是B,将燃着的木条放在瓶口,若观察到木条熄灭,说明瓶中已充满二氧化碳。
考点:实验室制取气体的思路和方法

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案某钙片的标签如下,且知钙片成分中只有碳酸钙中含有钙元素:

(1)(2分)请计算碳酸钙中钙元素的质量分数为 ;
(2)(2分)请通过计算推断此标签中的含钙量是 (填虚假或真实)的;
(3)(6分)某实验小组为测定其真实的含钙量做了如下实验,每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生的化学反应是:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,充分反应后再称取烧杯和剩余物质的总质量,数据如下:
物质的质量 | |
反应前:烧杯+盐酸 | 22g |
10片钙片 | 8g |
反应后:烧杯+剩余物 | 26.7g |
请计算此钙片中碳酸钙的质量分数。