题目内容
14.某工厂的废渣中混有少量的锌粉和氧化铜(其他的成分不跟酸反应),这些废渣与废盐酸接触时会形成有毒污水.若向污水中撒入铁粉,且反应后让铁粉有剩余,此时污水中一定含有的阳离子是( )| A. | Fe2+、Cu2+ | B. | Cu2+、H+ | C. | Zn2+、Fe2+、H+ | D. | Zn2+、Fe2+ |
分析 根据氧化铜和锌粉的废渣与废盐酸混合后会生成氯化铜与氯化锌,加入铁粉由于铁的活动性比铜强所以可以置换出溶液中的铜,据此分析解答即可.
解答 解:当混有少量的锌粉和氧化铜废渣与废盐酸接触时,氧化铜与锌都可以与盐酸反应生成氯化锌和氯化铜;向污水中撒入铁粉,因为铁的活动性比铜强所以可以置换出氯化铜溶液中的铜而生成氯化亚铁,若有剩余的盐酸,盐酸与铁反应生成了氯亚铁和氢气.由于铁粉过量,所以溶液中一定不会存在氯化铜、盐酸,由于铁的活动性比锌弱,所以不会置换出氯化锌溶液中的锌,溶液中一定含有的溶质是ZnCl2、FeCl2,因此溶液中含有的金属离子是Zn2+、Fe2+.
故选D.
点评 此题是对金属活动性顺序的考查,解题时可依据金属活动性顺序的意义解决.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.完成下列化学实验后,溶液的pH变大的是( )
| A. | 向含有酚酞的氢氧化钠溶液中滴加入盐酸,溶液变为无色 | |
| B. | 用稀硫酸与锌粒反应制取氢气 | |
| C. | 蒸发海水析出食盐 | |
| D. | 向石灰水中通入二氧化碳气体 |
19.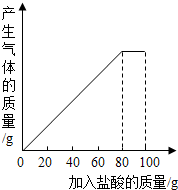 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.
请计算:
(1)第2次加入盐酸后,a为25g.
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为多少?10:3:22.
(3)求所用盐酸的质量分数?
 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)第2次加入盐酸后,a为25g.
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为多少?10:3:22.
(3)求所用盐酸的质量分数?
3.世界卫生组织(WHO)提出的空气质量指标如下表所示:(达到指标值可认为被空气污染,超过指标值为较重污染),已知成年人每天吸入空气约为14m3.计算:
(1)从上表中可知二氧化硫指标每立方米超过400×10-6g可认为空气被较重污染.
(2)每个成年人在没被污染的空气中,每天吸入氧气的体积约为2.9或2.8立方米(精确到0.1).
| 污染物 | 指标/10-6gm-3 | 污染物 | 指标/10-6gm-3 | |
| 二氧化硫 | 5-400 | 二氧化氮 | 10-150 | |
| 一氧化碳 | 500-700 | 铅 | 0.01-2 |
(2)每个成年人在没被污染的空气中,每天吸入氧气的体积约为2.9或2.8立方米(精确到0.1).
4.下列物质的用途主要是由物理性质决定的是( )
| A. | 氮气作保护气 | B. | 干冰作制冷剂 | C. | 天然气作燃料 | D. | 氧气用于炼钢 |
 将Fe2O3和纯净的碳粉混合平铺在反应管a中,锥形瓶b盛有足量澄清石灰水按图连接仪器.实验开始时缓慢通入氮气,过一段时间后,加热反应管,观察到管内发生剧烈反应,同时瓶中的溶液出现白色沉淀,待反应完成后停止加热,仍继续通入氮气直至反应管冷却.此时管内的混合物变成黑色粉末.回答问题:
将Fe2O3和纯净的碳粉混合平铺在反应管a中,锥形瓶b盛有足量澄清石灰水按图连接仪器.实验开始时缓慢通入氮气,过一段时间后,加热反应管,观察到管内发生剧烈反应,同时瓶中的溶液出现白色沉淀,待反应完成后停止加热,仍继续通入氮气直至反应管冷却.此时管内的混合物变成黑色粉末.回答问题: