题目内容
10.实验室利用下列装置可以制取某些气体,请据图回答问题: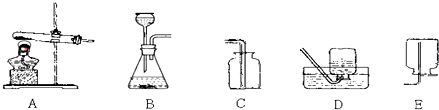
(1)这五个装置示意图中,有一个装置中有错误,该装置是B(填序号).
(2)氨气是一种无色、有刺激性气味的气体,密度比空气小,氨水显碱性.实验室里通过加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制得氨气,同时生成氯化钙和水.用化学方程式表示实验室制取氨气的化学反应原理:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(3)液氨泄漏时,可用喷水的方法除去空气中的氨气,说明氨气具有溶于水 的物理性质.
(4)实验室里选择上图中的A_做制取氨气的发生装置,理由是反应物是固体和反应需要加热.并选择E做氨气的收集装置.
(5)根据氨气的性质推测,发生液氨泄时,逃生的方法是:
①用湿毛巾捂住口鼻,②尽量贴近地面逃离(列举两条)
分析 (1)根据装配实验装置的注意事项来分析;
(2)根据制取氨气的反应,写出反应的化学方程式;
(3)根据液氨泄漏时,可用喷水的方法除去空气中的氨气,说明氨气具有溶于水的物理性质;
(4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置;
(5)根据发生液氨泄漏时正确的逃生方法是:用湿毛巾捂住口鼻;尽量贴近地面逃离解答.
解答 解:(1)装置B中的长颈漏斗下端没有伸入液面以下,生成的气体会从长颈漏斗逸出,故填:B;
(2)实验室里加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水.反应的化学方程式是:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;故填:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(3)液氨泄漏时,可用喷水的方法除去空气中的氨气,说明氨气具有溶于水的物理性质;故填:溶于水;
(4)用加热氯化铵和碱石灰固体混合物的方法制取氨气,应选择的发生装置是A;因密度比空气小,易溶于水,所以收集装置是D;故填:A;反应物是固体;反应需要加热;E;
(5)氨气溶于水,且密度比空气小,所以发生液氨泄漏时正确的逃生方法是:用湿毛巾捂住口鼻;尽量贴近地面逃离;故填:用湿毛巾捂住口鼻;尽量贴近地面逃离.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了安全注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列化学方程式书写正确的是( )
| A. | P+O2$\frac{\underline{\;点燃\;}}{\;}$ P2O5 | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2Fe2O3 | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑ | D. | 2Fe+3H2SO4═Fe2(SO4)3+H2↑ |
18.在一定温度下,将少量生石灰放入到一定量的饱和石灰水中,搅拌并冷却到原来的温度下列说法正确的是( )
| A. | 溶剂质量不变 | B. | 溶质质量变大 | C. | 溶液的浓度不变 | D. | 溶解度增大 |
5.下列混合物适宜用溶解、过滤、蒸发的方法进行分离的是( )
| A. | 食盐和白糖 | B. | 食盐和泥沙 | C. | 铁粉和铜粉 | D. | 二氧化碳和氧气 |
15.现有四种固体,分别是硫酸铜、氯化镁、氢氧化钠、氯化钠,不用其他试剂(水除外)能将四种物质鉴别开的顺序是( )
| A. | 硫酸铜、氯化镁、氢氧化钠、氯化钠 | B. | 硫酸铜、氢氧化钠、氯化镁、氯化钠 | ||
| C. | 硫酸铜、氯化镁、氯化钠、氢氧化钠 | D. | 氢氧化钠、硫酸铜、氯化镁、氯化钠 |
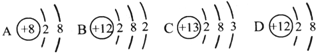
 构建知识网络是学习化学的重要方法之一,李明在学习酸、碱、盐后归纳并绘制出如图所示的物质之间的反应关系,(图中短线连接的物质表示能相互反应),请填写下列空白:
构建知识网络是学习化学的重要方法之一,李明在学习酸、碱、盐后归纳并绘制出如图所示的物质之间的反应关系,(图中短线连接的物质表示能相互反应),请填写下列空白: