题目内容
一包白色粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成.为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液.
(2)取(1)中滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体.根据上述实验可推断( )
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液.
(2)取(1)中滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体.根据上述实验可推断( )
| A、原固体混合物中一定不含有CuSO4、Na2SO4 |
| B、原固体混合物中一定不含有CuSO4、Na2SO4、BaCl2 |
| C、原固体混合物中一定含有CaCO3、NaOH |
| D、为进一步探究原白色粉末的组成,取(1)中得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl2、NaOH |
考点:物质的鉴别、推断,酸的化学性质,盐的化学性质
专题:混合物组成的推断题
分析:根据硫酸铜溶于水得到蓝色溶液,而本题中得到是无色的溶液,所以在混合物中一定不含硫酸铜,同时能形成白色沉淀的为碳酸钙,硫酸钠和氯化钡也可以反应生成白色沉淀,而白色沉淀能全部溶于稀硝酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀盐酸,所以该沉淀为碳酸钙,即硫酸钠和氯化钡最多含有一种,可以据此分析判断并解答该题.
解答:解:(1)把白色粉末溶解后得无色溶液,可知一定没有硫酸铜,因为硫酸铜溶于水会使溶液变蓝;
(2)实验(1)中的白色固体可能是碳酸钙,也可能是硫酸钠与氯化钡反应后生成的硫酸钡沉淀,但是硫酸钡不溶于水而且不溶于酸,而题目中的白色沉淀全部溶于稀盐酸中,并产生无色气体,说明这种白色沉淀是碳酸钙;
由实验(2)可以分析出硫酸钠和氯化钡只能存在一种,或者都不存在,所以根据(1)和(2)的条件可以得出可能组合为:①CaCO3 BaCl2;②CaCO3 BaCl2 NaOH;③CaCO3 Na2SO4;④CaCO3 Na2SO4 NaOH;⑤CaCO3 NaOH 故有5种可能;通入二氧化碳后产生了白色沉淀,根据题给条件这种白色沉淀只能是碳酸钡,但是二氧化碳不能与氯化钡反应生成沉淀,从而我们判断还应该有氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠后,碳酸钠与氯化钡反应生成了碳酸钡沉淀,故推断原白色粉末中还含有物质的BaCl2和NaOH,反应的方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl.综上所述,A、B、C都错误;
故选项为:D.
(2)实验(1)中的白色固体可能是碳酸钙,也可能是硫酸钠与氯化钡反应后生成的硫酸钡沉淀,但是硫酸钡不溶于水而且不溶于酸,而题目中的白色沉淀全部溶于稀盐酸中,并产生无色气体,说明这种白色沉淀是碳酸钙;
由实验(2)可以分析出硫酸钠和氯化钡只能存在一种,或者都不存在,所以根据(1)和(2)的条件可以得出可能组合为:①CaCO3 BaCl2;②CaCO3 BaCl2 NaOH;③CaCO3 Na2SO4;④CaCO3 Na2SO4 NaOH;⑤CaCO3 NaOH 故有5种可能;通入二氧化碳后产生了白色沉淀,根据题给条件这种白色沉淀只能是碳酸钡,但是二氧化碳不能与氯化钡反应生成沉淀,从而我们判断还应该有氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠后,碳酸钠与氯化钡反应生成了碳酸钡沉淀,故推断原白色粉末中还含有物质的BaCl2和NaOH,反应的方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl.综上所述,A、B、C都错误;
故选项为:D.
点评:本题属于文字叙述型推断题,在给定的物质范围和实验现象,来推出混合物中一定存在、一定不存在和可能存在的是什么物质;解答时以文字信息为序,寻找并抓住“题眼”,逐步分析“筛选”最终得出答案即可.

练习册系列答案
相关题目
下列家庭实验中不涉及化学变化的是( )
| A、用少量食醋除去水壶中的水垢 |
| B、用糯米、酒曲和水制甜酒酿 |
| C、光合作用 |
| D、用木炭除去冰箱中的异味 |
干冰易升华,下列关于此过程的说法正确的是( )
| A、分子质量变大 |
| B、分子间的间隔变大 |
| C、分子体积变大 |
| D、分子运动速率不变 |
关于“物质-在氧气中燃烧的主要现象--所属反应类型”的描述中正确的是( )
| A、碳--发出白光--化合反应 |
| B、硫--微弱淡蓝火焰--氧化反应 |
| C、铁--火星四射--分解反应 |
| D、蜡烛-发出白光,有水雾--氧化反应 |
生活中的下列做法利用了化学反应原理的是( )
| A、自制简易净水器净化自来水 |
| B、门锁不易打开时灌入铅笔芯粉末 |
| C、用液化石油气作燃料煮饭 |
| D、用活性炭除去冰箱中的异味 |
下列物质中,属于纯净物的是( )
| A、汽水 | B、水银 | C、石灰水 | D、牛奶 |
我国科学家研制出一种催化剂,能在室温下高效催化空气中一种有毒气体,其反应如图:下列说法,正确的是( )
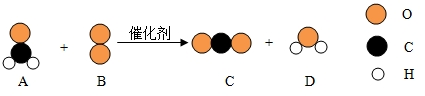

| A、该反应属于置换反应 |
| B、这种有毒气体的化学式为HCHO |
| C、其中有三种物质属于氧化物 |
| D、该反应中A与C的质量比为1:1 |
 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.