题目内容
7.实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究,请回答有关问题: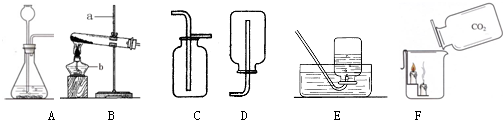
(1)请写出图中标有字母的仪器名称:a铁架台 b酒精灯
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气时,应选用的发生装置是A(填写装置的字母代号,下同),请写出该反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰起催化作用.
(3)实验室制取二氧化碳气体时,应选择的发生装置是A,应选择的收集装置是C,验证用该装置收集二氧化碳已满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.
(4)请写出实验室制取二氧化碳气体的化学方式:CaCO3+2HCl=CaCl2+H2O+CO2↑,用澄清石灰水检验二氧化碳时发生反应的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(5)如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是二氧化碳既不能燃烧、也不能支持燃烧且密度比空气的大,因此,二氧化碳可用于灭火.
分析 铁架台是常用的夹持仪器,酒精灯是常用的加热仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,其中二氧化锰起催化作用;如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是:二氧化碳既不能燃烧、也不能支持燃烧且密度比空气的大,因此,二氧化碳可用于灭火.
解答 解:(1)铁架台是常用的夹持仪器,酒精灯是常用的加热仪器,故答案为:铁架台;酒精灯;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,其中二氧化锰起催化作用,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:A;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;催化;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:A;C;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
(4)碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;Ca(OH)2+CO2=CaCO3↓+H2O;
(5)如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是:二氧化碳既不能燃烧、也不能支持燃烧且密度比空气的大,因此,二氧化碳可用于灭火;故答案为:二氧化碳既不能燃烧;也不能支持燃烧;灭火;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满和检验方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案| A. | 图书馆内图书着火,立即用高压水枪来灭火 | |
| B. | 将粉末状煤做成蜂窝煤,目的是增大煤与空气的接触面积,使燃烧更充分 | |
| C. | 用扇子扇煤炉火焰,越扇越旺,是因为提供了更充足的氧气 | |
| D. | 菜锅里的油着火时可以用锅盖盖灭,因为隔绝了空气 |
| 物 质 | 方法 |
| A.C(CuO) | 通入足量的CO后加热 |
| B.CaCl2溶液(HCl) | 加入过量Ca(OH)2溶液,使其充分反应 |
| C.CuSO4(H2SO4) | 加入过量CuO粉末,充分反应后过滤 |
| D.CO2(CO) | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | CO2能灭火,既利用了CO2的物理性质又利用了CO2的化学性质 | |
| C. | 碱溶液能使酚酞变红,所以能使酚酞变红的试液一定是碱溶液 | |
| D. | 酸性溶液的pH<7,所以pH<7的雨水是酸雨 |
①用加入三聚氰胺来提高奶粉的含氮量
②用福尔马林(甲醛的水溶液)浸泡海鲜产品来保鲜
③用小苏打(碳酸氢钠)发面做馒头使其松软可口
④用硫磺熏制生姜或种植时使用农药神农丹.
| A. | ①③ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
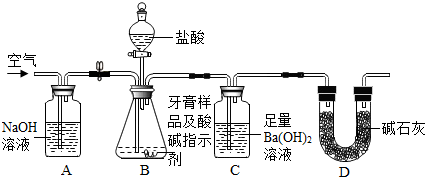
依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收
(2)下列各项措施中,不能提高测定准确度的是cd(填标号).
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(3)实验中准确称取8.00g样品四份,进行四次测定,每份测得BaCO3质量见表,则计算时所用BaCO3的质量为3.94g.
| BaCO3的质量/g | |
| 第一份 | 3.94 |
| 第二份 | 1.10 |
| 第三份 | 3.93 |
| 第四份 | 3.95 |
| A. |  苹果腐烂 | B. |  榨取果汁 | C. |  面包发霉 | D. |  菜刀生锈 |
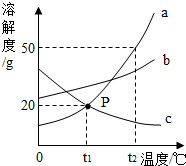 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答: