题目内容
在2A+B═2C中,6gA与一定量B完全反应,生成14gC,若B的相对分子质量32,则C的相对分子质量是
.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据质量守恒定律确定参加化学反应中B和C的质量比,然后结合化学方程式可解答本题.
解答:解:根据质量守恒定律,参加反应的B的质量为:14g-6g=8g
设C的相对原子质量为x
2A+B═2C
32 2x
8g 14g
=
x=28
答案:28
设C的相对原子质量为x
2A+B═2C
32 2x
8g 14g
| 32 |
| 8g |
| 2x |
| 14g |
x=28
答案:28
点评:在化学方程式计算时,计算质量时与化学式前面的系数无关,在计算相对分子质量时,与化学式前面的系数是有关的,这是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
合成材料的出现是材料发展史上的一次重大突破.下列物质中属于合成材料的是( )
| A、铝合金 | B、木工三合板 |
| C、汽车轮胎 | D、复合肥 |
下列现象能用质量守恒定律解释的是( )
| A、水结冰前后质量不变 |
| B、1升芝麻和1升大米混合,总体积小于2升 |
| C、在加压降温的条件下,氧气变为淡蓝色液体 |
| D、电解水时,生成的氢气和氧气的质量和与分解了的水的质量相等 |
下列变化属于物理变化的是( )
| A、菜刀生锈 | B、水分蒸发 |
| C、烟花燃放 | D、大米酿酒 |
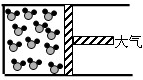 如图表示封闭在某容器中的少量液态水的微观示意图(该容器的活塞可以左右移动).煮沸后,液态水变成水蒸气.在这一过程中,发生的变化是( )
如图表示封闭在某容器中的少量液态水的微观示意图(该容器的活塞可以左右移动).煮沸后,液态水变成水蒸气.在这一过程中,发生的变化是( )| A、水分子 |
| B、水分子之间的间隔变大 |
| C、水分子的数目增多 |
| D、水分子受热都跑到容器的一端 |

 小民同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡有快有慢,于是他与小芳同学一起合作进行如下探究.
小民同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡有快有慢,于是他与小芳同学一起合作进行如下探究.