题目内容
1.在烧杯里加入10g的石灰石和足量的稀盐酸,充分反应后,烧杯内剩余物的质量比原来石灰石和稀盐酸的质量总和减少2.2g,计算:(1)生成二氧化碳的质量是多少?
(2)参加反应的碳酸钙的质量是多少?
(3)计算该石灰石的纯度(碳酸钙在石灰石中的质量分数)
分析 分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,因此,可知恰好完全反应时放出二氧化碳的质量为2.2g;然后利用二氧化碳的质量,根据反应的化学方程式,计算反应时碳酸钙的质量,进而求出该石灰石的纯度即可.
解答 解:(1)反应后烧杯里剩余物质的质量比原来石灰石和稀盐酸的质量之和减少的部分即是二氧化碳的质量,也就是生成的二氧化碳质量是2.2g;
(2)设生成2.2g二氧化碳时消耗碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
(3)该石灰石的纯度=$\frac{5g}{10g}×100%$=50%
答:(1)生成CO2气体的质量是2.2g;(2)参加反应的碳酸钙的质量是5g;(3)该石灰石的纯度为50%.
点评 掌握利用化学方程式计算的方法和步骤;注意从题目中寻找已知量和未知量,从而确定比例关系是解题的关键所在.

练习册系列答案
相关题目
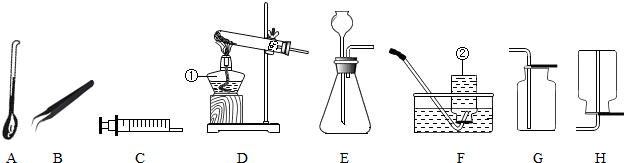
12.下列实验基本操作中,错误的是( )
| A. | 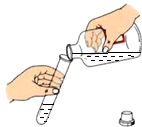 液体的倾倒 | B. | 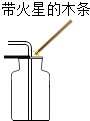 检验氧气是否集满 | ||
| C. | 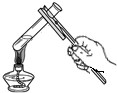 给液体加热 | D. | 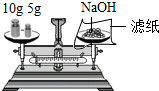 称取一定质量的NaOH |
16.已知化学方程式 X+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 下列对X的判断正确的是( )
| A. | 只含有C、H | B. | 一定含有C、H、O | ||
| C. | 可能C、H、O都含有 | D. | 一定含有C、H 可能含有O |
13.化学实验过程中要规范操作,注意实验安全,如果发生意外也要冷静处理.下列意外事故的处理方法中,正确的是( )
| 选项 | 意外事故 | 处理方法 |
| A | 洒在桌面上的酒精燃烧起来 | 立即撤离实验室 |
| B | 氢氧化钠溶液沾在皮肤上 | 用水冲洗后,再涂上3%~5%的碳酸氢钠溶液 |
| C | 浓硫酸沾在皮肤上 | 用水冲洗后,再涂上氢氧化钠溶液 |
| D | 实验药品溅到眼睛里 | 用水冲洗,一边洗一边眨眼睛,然后送医院 |
| A. | A | B. | B | C. | C | D. | D |
10.下列区分物质的方法不正确的是( )
| A. | 硬水、软水--加肥皂水,观察泡沫产生情况 | |
| B. | 氢氧化钠溶液、碳酸钠溶液--加入酚酞试液,观察溶液是否变色 | |
| C. | 澄清石灰水、稀H2SO4、NaCl溶液,用Na2CO3溶液就能把他们一次区别开来 | |
| D. | 棉纤维、羊毛纤维--点燃,闻是否有烧焦羽毛的气味 |
11.下列物品中所用的材料属于有机合成材料的是( )
| A. | 纯棉T恤 | B. | 塑料薄膜 | C. | 蚕丝被 | D. | 羊绒背心 |
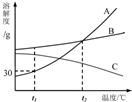 图是A、B、C三种物质的溶解度曲线,据图回答:
图是A、B、C三种物质的溶解度曲线,据图回答: