题目内容
现有114.5g稀硫酸,经测定其中含有氢元素共10.5g,问稀硫酸中含硫酸和水各多少克?
考点:混合物中某元素的质量计算
专题:化学式的计算
分析:稀硫酸是硫酸的水溶液,设含硫酸的质量为x,则含水的质量为114.5g-x,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:稀硫酸是硫酸的水溶液,设含硫酸的质量为x,则含水的质量为114.5g-x,经测定其中含有氢元素共10.5g,
则x×
×100%+(114.5g-x)×
×100%=10.5g x=24.5g.
含水的质量为114.5g-24.5g=90g.
答:稀硫酸中含硫酸和水的质量分别是24.5g、90g.
则x×
| 1×2 |
| 98 |
| 1×2 |
| 18 |
含水的质量为114.5g-24.5g=90g.
答:稀硫酸中含硫酸和水的质量分别是24.5g、90g.
点评:本题难度不大,掌握化合物中某元素的质量=该化合物的质量×该元素的质量分数并能灵活运用是正确解答本题的关键.

练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
不能在酒精灯火焰上加热的仪器是( )
| A、试管 | B、燃烧匙 |
| C、蒸发皿 | D、量筒 |
对于反应A+B═C+D来说,下列说法错误的是( )
| A、A、B、C、D中可能有一种是气体 |
| B、若参加反应的A、B分别为10克,则C、D质量的和≤20克 |
| C、A、C可能是单质,B、D可能是化合物 |
| D、A和B质量之比等于C和D质量之比. |
把X、Y、Z三种金属片分别加入稀硫酸中,X、Y表面有气泡产生,Z无变化;把X加入Y的硫酸盐溶液中,X表面析出Y.则三种金属活动顺序为( )
| A、X>Y>Z |
| B、Y>X>Z |
| C、Z>Y>X |
| D、X>Z>Y |
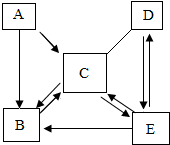 已知A,B,C,D,E是初中化学中已学过的常见的五种物质,其中物质A是一种黑色固体单质,B,C,E是无色气体,且B,C两种气体组成元素相同,D在常温下是一种无色液体,它们在一定条件下关系如图所示,(反应条件已略去,断线“-”表示相连物质间能发生反应,箭头“→”表示物质间可转化).是推断并回答相关问题:
已知A,B,C,D,E是初中化学中已学过的常见的五种物质,其中物质A是一种黑色固体单质,B,C,E是无色气体,且B,C两种气体组成元素相同,D在常温下是一种无色液体,它们在一定条件下关系如图所示,(反应条件已略去,断线“-”表示相连物质间能发生反应,箭头“→”表示物质间可转化).是推断并回答相关问题: