题目内容
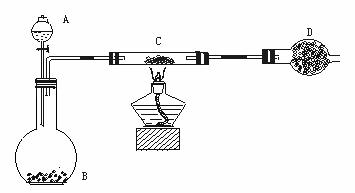 某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图所示装置,对获得的铜粉(含炭)样品进行实验,测定铜的质量分数。图中铁架台等装置已略去。请回答下列问题:
某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图所示装置,对获得的铜粉(含炭)样品进行实验,测定铜的质量分数。图中铁架台等装置已略去。请回答下列问题:
仪器:铁架台(含铁圈、铁夹)、分液漏斗、平底烧瓶、硬质玻璃管、干燥管、酒精灯、石棉网、洗气瓶等。
药品:红褐色(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰(固体氢氧化钠和氧化钙的混合物,可用来吸收水和CO2)。
①除上述仪器外,实验中还必须用到的仪器是(30) ;
②实验操作前,首先进行(31) 检查。在C中加入样品粉末W g,D中装入药品后并称量为m1 g,连接好仪器。打开A的上塞、活塞,慢慢滴加溶液。对C进行加热。当C中药品充分反应后,关闭A的活塞,停止加热。冷却后,称量D的质 量为m2 g。
量为m2 g。
实验进行的过程中,装置C中发生的主要化学反应类型(32) ;充分反应后装置C中剩余的固体成分是(33) 。
③问题和讨论:
 实验完成后,老师评议说:按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与C之间加入一个装置,该装置作用是(34) 。
实验完成后,老师评议说:按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与C之间加入一个装置,该装置作用是(34) 。
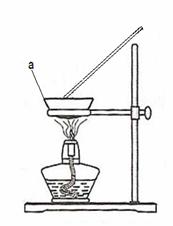
④有学生提出直接用右图装置,在空气中直接加热进行实验。
图中仪器“a”的名称为 (35) 。
若取20g铜粉(含炭)样品进行实验,充分反应后,仪器a中
剩余的固体质量为24g,计算求原来混合物中铜的物质的量以
及铜的质量分数。
(要求:根据化学方程式计算,并写出计算过程!)
(3 6)
6)
| 天平 | 1 | |
| (31) | 气密性 | 1 |
| (32) | 化合反应 | 1 |
| (33) | 氧化铜 | 1 |
| (34) | 干燥 | 1 |
| (35) | 蒸发皿 | 1 |
| (36) | 解:设生成硫酸铜质量为x克 2Cu+O2 | 1 |
| 128
| 1 | |
| x=19.2 n(Cu)=19.2/64=0.3mol | 1 | |
| 铜的质量分 答:略 | 1 |

在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示。下列未知数据计算正确的是 【 】
| 物 质 | a | b | c | d |
| 反应前的质量(g) | 10 | 10 | 0 | 0 |
| 反应中的质量(g) | 6 | 2 | 3 | ① |
| 反应后的质量(g) | ② | 0 | ③ | ④ |
A.①为7  B.②为6 C.③3.75
B.②为6 C.③3.75  D.④16.25
D.④16.25
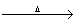 2CuO
2CuO X 24
X 24 水资源非常短缺,所以在生产和生活中应该( )
水资源非常短缺,所以在生产和生活中应该( )