题目内容
5.对钠原子和钠离子的叙述错误的是( )| A. | 都属于钠元素 | B. | 化学性质相同 | ||
| C. | 钠离子比钠原子少一个电子 | D. | 核电荷数相同 |
分析 根据钠原子和钠离子的结构来分析它们的核电荷数、电子数、电子层数之间的关系.
解答 解:A、Na+是钠原子失去一个电子后形成的,质子数没有改变,所以钠原子、钠离子具有相同的质子数,都属于钠元素,故正确;
B、Na+是钠原子失去一个电子后形成的,所以二者的核外电子数不同,化学性质不相同,故错误;
C、Na+是钠原子失去一个电子后形成的,钠离子比钠原子少一个电子,所以二者的核外电子数不同,故错误;
D、Na+是钠原子失去一个电子后形成的,质子数没有改变,所以钠原子、钠离子具有相同的质子数,而质子数=核电荷数,正确;
故选:B.
点评 本题考查原子和离子的转化及它们的性质的分析,学生应能从微粒的结构的角度来分析,明确原子和离子之间的转化是解答的关键.

练习册系列答案
相关题目
6. 在“宏观-微观-符号”之间建立联系,是学习化学的一种重要的思维方式.如图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列的问题.
在“宏观-微观-符号”之间建立联系,是学习化学的一种重要的思维方式.如图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列的问题.
(1)硒原子结构示意图中的X=8,硒元素属于非金属(填“金属”或“非金属”)元素.
(2)硬水中含有的金属离子为Ca2+;Mg2+(填离子符号)
(3)硫元素和硒元素的化学性质相似,所以硒酸的化学式为H2SeO4.
(4)相对分子质量与标准状况下的气体体积之间存在紧密的关系(见下表),根据下表判断,
标准状况下22.4L氮气的质量Y为28g.请根据下表归纳出一条规律:标准状况下,22.4L气体的质量数值上等于其相对分子质量.
 在“宏观-微观-符号”之间建立联系,是学习化学的一种重要的思维方式.如图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列的问题.
在“宏观-微观-符号”之间建立联系,是学习化学的一种重要的思维方式.如图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列的问题.(1)硒原子结构示意图中的X=8,硒元素属于非金属(填“金属”或“非金属”)元素.
(2)硬水中含有的金属离子为Ca2+;Mg2+(填离子符号)
(3)硫元素和硒元素的化学性质相似,所以硒酸的化学式为H2SeO4.
(4)相对分子质量与标准状况下的气体体积之间存在紧密的关系(见下表),根据下表判断,
| 氢气 | 氧气 | 氮气 | |
| 相对分子质量 | 2 | 32 | 28 |
| 标准状况下,22.4L气体的质量 | 2g | 32g | Y |
16.部分变质的氢氧化钙样品24.8g,待其完全变质后,加入到200g稀盐酸中恰好完全反应,得到溶液216.8g,则原样品的变质程度为( )
| A. | 33.3% | B. | 66.7% | C. | 80% | D. | 74% |
20.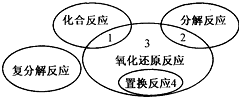 在化学反应中,反应前后元素化合价发生变化的反应就是氧化还原反应.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是( )
在化学反应中,反应前后元素化合价发生变化的反应就是氧化还原反应.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是( )
 在化学反应中,反应前后元素化合价发生变化的反应就是氧化还原反应.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是( )
在化学反应中,反应前后元素化合价发生变化的反应就是氧化还原反应.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是( )| A. | Fe2O3+3H2SO4═Fe2(SO4)3+3H2O | B. | NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ | ||
| C. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | Fe+2HCl═FeCl2+H2↑ |
10.实验是学习化学的一条重要途径.下列化学实验操作正确的是( )
| A. | 用滴管向试管内加入少量液体 | |
| B. | 用手捂住试管检验装置气密性 | |
| C. | 将燃着的木条伸入集气瓶中检验二氧化碳是否收集满 | |
| D. | 将浓硫酸沿着烧杯内壁慢慢倒入水中,并用玻璃棒搅拌 |
17.化学知识在生活中有着广泛的应用,下列说法不正确的是( )
| A. | 血红蛋白质中含有铁元素,缺铁会引起人体贫血 | |
| B. | 回收废弃的塑料可以减少白色污染 | |
| C. | NaCl和NaNO2有咸味,都可用作食物的调味品 | |
| D. | 在发酵的面团中加入小苏打以提高馒头的口感和除去酸味 |