题目内容
15.取12g石灰石样品与烧杯中,向其中加入100g溶质质量分数为7.3%的稀盐酸可以恰好完全反应,计算:(1)该反应过程中生成的气体的质量4.4g;
(2)该石灰石样品中CaCO3的质量分数为多少?(写出计算过程,结果保留一位小数)
分析 根据盐酸的质量、质量分数可以计算生成二氧化碳的质量、碳酸钙的质量,进一步可以计算石灰石中CaCO3的质量分数.
解答 解:100g溶质质量分数为7.3%的稀盐酸中溶质的质量为:100g×7.3%=7.3g
设生成二氧化碳的质量为x,石灰石中碳酸钙的质量为y,
CaCO3 +2HCl═CaCl2+H2O+CO2↑,
100 73 44
y 7.3g x
$\frac{44}{x}$=$\frac{100}{y}$=$\frac{73}{7.3g}$
解得:x=4.4g y=10g
(2)该石灰石样品中碳酸钙的质量分数为:$\frac{10g}{12g}$×100%≈83.3%
答:该石灰石样品中CaCO3的质量分数为83.3%.
故答案为:(1)4.4g;
(2)83.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
相关题目
16.下列图示的实验基本操作不正确的是( )
| A. |  | B. |  | C. |  | D. |  |
6. 化学反应的多角度认识
化学反应的多角度认识
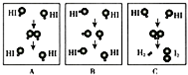
(1)在化学反应中,反应物分子间相互碰撞是反应进行的必要条件,但不是每一次碰撞都能发生化学反应.如图为碘化氢(HI)分子之间的几种碰撞示意图,有些碘化氢分子碰撞后,会发生化学反应产生H2和I2,有些碰撞不会发生反应.
①A、B、C三图中表示碘化氢分子碰撞后发生了化学反应的是图C(填字母序号).
②若要得到一个氢分子,至少需要2个碘化氢分子碰撞.
③上述发生的反应属于分解反应.
④分析反应过程可知,化学反应的实质是分子分成了原子,原子重新组合成新的分子.
(2)化学反应速率会受到浓度、压强、温度、催化剂等因素的影响.
某化学小组为了研究外界条件对化学反应速率的影响,用4mL一定质量分数的KMnO4溶液(紫色)与2mL一定质量分数的H2C2O4溶液进行实验,研究不同条件对化学反应速率的影响.改变的条件如下:
已知:2KMnO4+5H2C204+3H2S04=K2SO4+2MnS04(肉色)+l0CO2↑+8H20
①如果研究催化剂对化学反应速率的影响,使用实验I和Ⅱ(用I~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验I和Ⅲ.
②对比实验I和Ⅳ,可以研究反应物的浓度对化学反应速率的影响,实验Ⅳ中加人1mL蒸馏水的目的是确保溶液的体积相等,其反应物浓度一致.
 化学反应的多角度认识
化学反应的多角度认识(1)在化学反应中,反应物分子间相互碰撞是反应进行的必要条件,但不是每一次碰撞都能发生化学反应.如图为碘化氢(HI)分子之间的几种碰撞示意图,有些碘化氢分子碰撞后,会发生化学反应产生H2和I2,有些碰撞不会发生反应.
①A、B、C三图中表示碘化氢分子碰撞后发生了化学反应的是图C(填字母序号).
②若要得到一个氢分子,至少需要2个碘化氢分子碰撞.
③上述发生的反应属于分解反应.
④分析反应过程可知,化学反应的实质是分子分成了原子,原子重新组合成新的分子.
(2)化学反应速率会受到浓度、压强、温度、催化剂等因素的影响.
某化学小组为了研究外界条件对化学反应速率的影响,用4mL一定质量分数的KMnO4溶液(紫色)与2mL一定质量分数的H2C2O4溶液进行实验,研究不同条件对化学反应速率的影响.改变的条件如下:
| 实验 | 硫酸(10%)体积/mL | 温度/℃ | 其他物质 |
| I | 2mL | 20 | / |
| Ⅱ | 2mL | 20 | 10滴饱和MnS04溶液 |
| Ⅲ | 2mL | 30 | / |
| Ⅳ | 1mL | 20 | 1mL蒸馏水 |
①如果研究催化剂对化学反应速率的影响,使用实验I和Ⅱ(用I~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验I和Ⅲ.
②对比实验I和Ⅳ,可以研究反应物的浓度对化学反应速率的影响,实验Ⅳ中加人1mL蒸馏水的目的是确保溶液的体积相等,其反应物浓度一致.
3.某同学记录的实验数据,其中不合理的是( )
| A. | 用天平称取2.5克食盐 | B. | 用10毫升量筒量取8.3毫升水 | ||
| C. | 用50毫升烧杯量取28.13毫升水 | D. | 用50毫升烧杯量取约30毫升水 |
10.在4A+3B═2C+5D,当20g A和35g B恰好完全反应后,生成5g D.若A的相对分子质量为20,C的相对分子质量为( )
| A. | 50 | B. | 25 | C. | 100 | D. | 200 |
7.按体积计算,空气中含量最多、且能充入食品袋里防腐的物质是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 水蒸气 |
4.若将4克氧化铜用氢气还原成铜,实际消耗氢气的质量一定( )
| A. | 等于0.1克 | B. | 大于0.1克 | C. | 小于0.1克 | D. | 无法确定 |
