题目内容
17.在Cu(NO3)2、AgNO3、Mg(NO3)2的混合溶液中,加一定量的锌粒,充分反应过滤,向滤出固体中滴加稀硫酸.(1)若有气泡产生,则滤出的固体物质中一定有银、铜、锌,滤液中一定有硝酸镁、硝酸锌.
(2)若没有气泡产生,则滤出固体物质中一定有银,可能有铜;滤液中一定有硝酸镁、硝酸锌,可能有硝酸银和硝酸铜.
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此进行分析解答.
解答 解:根据在金属活动性顺序中,镁>锌>氢>铜>银,故锌不能与Mg(NO3)2溶液反应,锌先与硝酸银反应生成银和硝酸锌溶液,硝酸银溶液反应完,若还有锌,再与硝酸铜溶液反应生成铜和硝酸锌溶液.
(1)充分反应过滤,向滤出固体中滴加稀硫酸,若有气泡产生,说明有能与稀硫酸反应的金属存在,这种金属应是锌,说明锌是过量的,则滤出的固体物质中一定有银、铜、锌;滤液中一定有硝酸镁、硝酸锌.
(2)充分反应过滤,向滤出固体中滴加稀硫酸,若无气泡产生,说明滤渣中的金属不与稀硫酸反应,则可能是锌只与硝酸银反应生成银和硝酸锌溶液,也可能是锌与硝酸银、硝酸铜均发生了反应(可能与硝酸铜溶液只反应了一部分,或恰好完全反应),但一定没有锌剩余,则滤出的固体物质中一定有银,可能含有铜;滤液中一定有生成的硝酸锌、没有参加反应的Mg(NO3)2,可能含有硝酸银和硝酸铜.
故答案为:(1)银、铜、锌;硝酸镁、硝酸锌;
(2)银;铜;硝酸镁、硝酸锌;硝酸银和硝酸铜.
点评 本题难度不是很大,熟练掌握金属的化学性质、综合考虑各种出现的情况是正确解答此类题的关键.

练习册系列答案
相关题目
20.如表有关物质除杂、分离、区分所用的试剂或方法都正确的( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去NaCl溶液中少量Na2CO3 | 适量澄清石灰水、过滤 |
| B | 除去二氧化碳中混有的水蒸气 | 通入装有生石灰的干燥管 |
| C | 从高锰酸钾制氧气的残余物中分离出MnO2 | 加水溶解、过滤、洗涤、干燥 |
| D | 区分失去标签的稀盐酸和稀硫酸 | 紫色石蕊溶液或铁粉 |
| A. | A | B. | B | C. | C | D. | D |
5.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四,理由是H2SO4和NaOH在溶液中不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四,理由是H2SO4和NaOH在溶液中不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  | 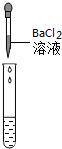 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
12.学校化学兴趣小组在学习金属化学性质后,作了以下探究实验.
(1)小董将铜丝放入硝酸银溶液中,该反应的化学方程式为Cu+2AgNO3═2Ag+Cu(NO3)2.
(2)小凡将锌粒放入一定量的硝酸银溶液中,发现反应后溶液的质量变小(填“变大”、“变小”或“不变”).
(3)小晗在思考:如果将铜粉与锌粉的混合物放入一定量的硝酸银溶液中,反应是否有先后顺序?探究如下:
【提出问题】铜粉与锌粉的混合物放入一定量的硝酸银溶液中,反应是否有先后顺序?
【作出猜想】①铜粉先与硝酸银溶液反应 ②锌粉先与硝酸银溶液反应
【设计实验】①小晗取一定量铜粉和锌粉的混合物,放入少量的硝酸银溶液中,溶液的颜色没有发生变化,由此推断:铜粉与硝酸银溶液没有(填“发生”或“没发生”)反应.然后再向反应后的混合物中加入稀硫酸,发现无气泡产生,由此推断:锌粉与硝酸银溶液发生(填“发生”或“没发生”)反应.
②小晗再取同样的铁粉和锌粉混合物放入较多量的硝酸银溶液中,看到溶液变成蓝色,由此推断铜粉与硝酸银溶液发生(填“发生”或“没发生”)反应.
【分析并得出结论】综合上述实验现象可知,铜粉与锌粉的混合物放入一定量的硝酸银溶液中,锌粉优先与硝酸银溶液反应.
【反思】小晗分析得到蓝色溶液,对溶液中所含的溶质做出多种猜想,其中有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为硝酸锌、硝酸铜和硝酸银.
(4)在探究实验后,为了测定某稀硫酸的质量分数,他们取铜粉和锌粉的混合物10克放入烧杯中,再取60克稀硫酸分6次加入烧杯中,均充分反应,实验数据如下:
根据上表提供的数据,求所用稀硫酸的质量分数.
(1)小董将铜丝放入硝酸银溶液中,该反应的化学方程式为Cu+2AgNO3═2Ag+Cu(NO3)2.
(2)小凡将锌粒放入一定量的硝酸银溶液中,发现反应后溶液的质量变小(填“变大”、“变小”或“不变”).
(3)小晗在思考:如果将铜粉与锌粉的混合物放入一定量的硝酸银溶液中,反应是否有先后顺序?探究如下:
【提出问题】铜粉与锌粉的混合物放入一定量的硝酸银溶液中,反应是否有先后顺序?
【作出猜想】①铜粉先与硝酸银溶液反应 ②锌粉先与硝酸银溶液反应
【设计实验】①小晗取一定量铜粉和锌粉的混合物,放入少量的硝酸银溶液中,溶液的颜色没有发生变化,由此推断:铜粉与硝酸银溶液没有(填“发生”或“没发生”)反应.然后再向反应后的混合物中加入稀硫酸,发现无气泡产生,由此推断:锌粉与硝酸银溶液发生(填“发生”或“没发生”)反应.
②小晗再取同样的铁粉和锌粉混合物放入较多量的硝酸银溶液中,看到溶液变成蓝色,由此推断铜粉与硝酸银溶液发生(填“发生”或“没发生”)反应.
【分析并得出结论】综合上述实验现象可知,铜粉与锌粉的混合物放入一定量的硝酸银溶液中,锌粉优先与硝酸银溶液反应.
【反思】小晗分析得到蓝色溶液,对溶液中所含的溶质做出多种猜想,其中有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为硝酸锌、硝酸铜和硝酸银.
(4)在探究实验后,为了测定某稀硫酸的质量分数,他们取铜粉和锌粉的混合物10克放入烧杯中,再取60克稀硫酸分6次加入烧杯中,均充分反应,实验数据如下:
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量 (g) | 9.35 | 8.70 | 8.05 | 7.40 | 6.75 | 6.75 |
6.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如表所示.下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前(%) | 70 | 14 | m | 10 |
| 反应后(%) | 42 | n | 40 | 10 |
| A. | 若消耗3 g乙,则生成17 g丙 | |
| B. | 丙可能是单质 | |
| C. | 丁一定是该反应的催化剂 | |
| D. | 甲、乙的质量之和一定等于生成丙的质量 |
7.分析推理是化学学习中常用的思维方法,下列说法正确的是( )
| A. | 离子都带有电荷,所以带有电荷的粒子一定是离子 | |
| B. | 不同种分子构成混合物,所以混合物一定有不同种分子构成 | |
| C. | 单质只含有一种元素,所以由一种元素组成的纯净物一定是单质 | |
| D. | 化合反应生成一种物质,所以生成一种物质的反应一定是化合反应 |
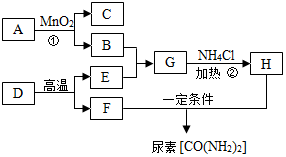 如图表示某些物质间转化关系.A、B为组成元素相同的无色液体,D是大理石的主要成分,C、F、H为气体,且H有刺激性气味.
如图表示某些物质间转化关系.A、B为组成元素相同的无色液体,D是大理石的主要成分,C、F、H为气体,且H有刺激性气味.