题目内容
4.某化学家设计了下列反应步骤:①CaBr2+H2O$\frac{\underline{\;700℃\;}}{\;}$CaO+2HBr ②2HBr+Hg$\frac{\underline{\;500℃\;}}{\;}$HgBr2+H2
③HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2④2HgO$\frac{\underline{\;100℃\;}}{\;}$2Hg+O2↑
你认为该方法的主要目的是为了获得氢气.请你评价一下这种方法有哪些缺陷耗能大,使用重金属会污染环境.
分析 由CaBr2+H2O$\frac{\underline{\;700℃\;}}{\;}$CaO+2HBr,2HBr+Hg$\frac{\underline{\;500℃\;}}{\;}$HgBr2+H2,HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2,2HgO$\frac{\underline{\;100℃\;}}{\;}$2Hg+O2↑可知,HgO+H2O=Hg+H2↑+O2↑.
解答 解:由CaBr2+H2O$\frac{\underline{\;700℃\;}}{\;}$CaO+2HBr,2HBr+Hg$\frac{\underline{\;500℃\;}}{\;}$HgBr2+H2,HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2,2HgO$\frac{\underline{\;100℃\;}}{\;}$2Hg+O2↑可知,HgO+H2O=Hg+H2↑+O2↑,因此该方法的主要目的是为了获得氢气,这种方法的缺陷是:耗能大,使用重金属会污染环境等.
故填:氢气;耗能大,使用重金属会污染环境.
点评 解答的关键是根据反应的化学方程式能够整合出HgO+H2O=Hg+H2↑+O2↑,下一步判断就比较简单了.

练习册系列答案
相关题目
14.2015年10月,屠呦呦因发现青蒿素(C15H22O5)而获得诺贝尔医学奖.青蒿素是抗疟的有效成分,它是一种无色晶体,可溶于乙醇、乙醚,几乎不溶于水.屠呦呦在提取青蒿素时,发现加热过程中会破坏青蒿里面的有效成分,于是改用乙醚提取.下列关于青蒿素的说法正确的是( )
| A. | 青蒿素中C、H、O三种元素的质量比为15:22:5 | |
| B. | 青蒿素是氧化物 | |
| C. | 用乙醚提取青蒿素利用了青蒿素的溶解性 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |
15.芋艿(俗称毛芋)是一种常见的食品,新鲜芋艿在去皮时会出现一种白色的汁液,汁液内含有一种碱性物质--皂角,沾上它会奇痒难忍.下列厨房中的物质止痒效果最好的是( )
| A. | 食醋 | B. | 料酒 | C. | 肥皂水 | D. | 食盐水 |
12.某同学收集生活中的物质建立家庭实验室,下表是该同学对这些物质分类存放的情况,请你在表中填写物质的类别(填“金属”、“氧化物”、“酸”、“碱”、“盐”、“有机物”):
| 物质类别 | (1)有机物 | 金属 | (2)碱 | 盐 |
| 物质 | 蔗糖、酒精 | 铜丝、铁丝 | 熟石灰 | 高锰酸钾 |
19.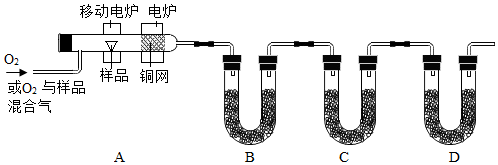 某化学研究小组以“烃类有机物中碳、氢元素的质量分数测定”为题进行了如图的实验设计.
某化学研究小组以“烃类有机物中碳、氢元素的质量分数测定”为题进行了如图的实验设计.
一定量样品和氧气混合气经过灼热的铜网时被充分氧化,产生二氧化碳和水蒸气.经B、C、D装置可以测得产生的二氧化碳和水蒸气的质量,进而推知样品中碳和氢元素的质量分数.
(1)产生的二氧化碳和水蒸气是否被充分吸收,会影响碳、氢元素的含量测定.研究小组的成员查找到了如表所示有关数据,试图了解吸收剂的吸收性能.如表是20℃时,1m3空气中经下列吸收剂吸收后水蒸气残留的克数:
根据表中数据,你认为吸收水蒸气时,最理想的吸收剂是Mg(ClO4)2固体.
(2)C中的药品为硫酸铜固体,C装置的作用是检验水蒸气是否被B装置完全吸收.B、D装置中的药品也为固体,你认为研究小组在这一实验中,B中药品为Mg(ClO4)2固体.D中药品为碱石灰.
(3)该装置测得二氧化碳的质量是否准确?为什么?不准确,这是因为D装置中的碱石灰能够吸收空气中的水蒸气和二氧化碳.
(4)某同学用如图装置测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,测得装置B、D两者分别增重0.144g和0.528g,生成物完全被吸收.维生素中是否含有氧元素?含有氧元素(试通过计算说明).
 某化学研究小组以“烃类有机物中碳、氢元素的质量分数测定”为题进行了如图的实验设计.
某化学研究小组以“烃类有机物中碳、氢元素的质量分数测定”为题进行了如图的实验设计.一定量样品和氧气混合气经过灼热的铜网时被充分氧化,产生二氧化碳和水蒸气.经B、C、D装置可以测得产生的二氧化碳和水蒸气的质量,进而推知样品中碳和氢元素的质量分数.
(1)产生的二氧化碳和水蒸气是否被充分吸收,会影响碳、氢元素的含量测定.研究小组的成员查找到了如表所示有关数据,试图了解吸收剂的吸收性能.如表是20℃时,1m3空气中经下列吸收剂吸收后水蒸气残留的克数:
| 吸收剂 | 浓硫酸 | Mg(ClO4)2固体 | CuSO4 | 硅胶 | CaO | NaOH |
| 残留质量 | 0.003 | 0.0005 | 1.4 | 0.03 | 0.2 | 0.14~0.25 |
(2)C中的药品为硫酸铜固体,C装置的作用是检验水蒸气是否被B装置完全吸收.B、D装置中的药品也为固体,你认为研究小组在这一实验中,B中药品为Mg(ClO4)2固体.D中药品为碱石灰.
(3)该装置测得二氧化碳的质量是否准确?为什么?不准确,这是因为D装置中的碱石灰能够吸收空气中的水蒸气和二氧化碳.
(4)某同学用如图装置测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,测得装置B、D两者分别增重0.144g和0.528g,生成物完全被吸收.维生素中是否含有氧元素?含有氧元素(试通过计算说明).
9.下列物质的应用主要是由化学性质决定的是( )
| A. | 稀有气体作霓虹灯 | B. | 分离液态空气得到氧气 | ||
| C. | 铝块压成薄片 | D. | 氮气用于食品包装填充气 |
16.以科学原理和实验事实为依据进行推理是学习化学的一种重要方法.下列推理得出的相关结论正确的是( )
| A. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| B. | 氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| C. | 铁丝在氧气中能够燃烧,空气中有氧气,所以铁丝在空气中一定能够燃烧 | |
| D. | 含碳元素的物质充分燃烧会生成CO2,所以燃烧能生成CO2的物质一定含碳元素 |
14. 向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法符合反应事实的是( )
向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法符合反应事实的是( )
 向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法符合反应事实的是( )
向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法符合反应事实的是( )| A. | 在0-a段发生3个化学反应 | B. | c点的沉淀是BaSO4 | ||
| C. | 图中m点的值是2.33g | D. | 在b-c段溶液中有2种溶质 |