题目内容
13.下列是钠元素、氯元素在元素周期表中的信息及有关粒子的结构示意图,请回答下列问题:
(1)D所表示的粒子是Na+(填化学符号),氯原子的结构示意图是E(填序号).
(2)D、F形成化合物的化学式是NaCl.
(3)与元素的化学性质关系最密切的是④(填序号).
①原子的核外电子数 ②元素的相对原子质量
③元素的原子序数 ④原子的最外层电子数.
分析 (1)根据粒子符号的写法以及原子结构示意图的画法来分析;
(2)根据化合物的化学式的写法来分析;
(3)根据决定元素化学性质的主要因素来分析.
解答 解:(1)微粒D的核内质子数为11,核外电子数为10,是带有1个单位正电荷的钠离子,符号为Na+;氯是17号元素,氯原子核内质子数为17,核外电子排布为2、8、7,所以E是氯原子结构示意图;故填:Na+;E;
(2)D是带有一个单位正电荷的钠离子,F是带有一个单位负电荷的氯离子,二者组成的化合物的化学式为NaCl;故填:NaCl;
(3)元素性质与原子核外电子的排布,特别是最外层上的电子数目有密切关系,所以决定元素化学性质的是最外层电子数,故填:④.
点评 本题通过给出微粒的模型考查了学生的观察能力和对基本概念的理解与运用能力;了解元素周期表的特点及其应用,以及核外电子在化学反应中的作用是解题的关键.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
3.木糖醇是一种甜味剂,其溶解度曲线如图所示.下列关于木糖醇的叙述中不正确的是( )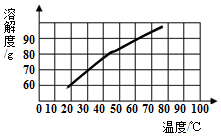

| A. | 木糖醇的溶解度随温度的升高而增大 | |
| B. | 木糖醇是易溶物质 | |
| C. | 70℃时木糖醇的饱和溶液降温到60℃会析出木糖醇晶体 | |
| D. | 50℃时,100g水中加入80g木糖醇,搅拌,可得到饱和溶液 |
4.下列实验操作正确的是( )
| A. | 用玻璃棒搅拌加快过滤 | |
| B. | 用镊子取用二氧化锰 | |
| C. | 用量筒量取液体时最后改用胶头滴管加至刻度 | |
| D. | 实验室模拟炼铁时先加热氧化铁再通一氧化碳 |
1.农作物种植过程中可以施用下列化肥,其中属于复合肥的是( )
| A. | NH4HCO3 | B. | KNO3 | C. | Ca(H2PO4)2 | D. | CO(NH2)2 |
8.有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化,根据以上实验事实,判断X、Y、Z三种金属的活动性由强到弱的顺序正确的是( )
| A. | X Y Z | B. | X Z Y | C. | Y Z X | D. | Z Y X |
5.常温下,一些食物的近似pH如下,其中酸性最强的是( )
| A. | 柠檬汁(2.1~2.8) | B. | 菠萝汁(3.3~5.2) | C. | 牛奶(6.3~6.6) | D. | 鸡蛋清(7.6~8.0) |
