题目内容
N(NO2)3是科学家2011年发现的一种新型火箭燃料.请按要求进行计算:
(1)N(NO2)3中氮元素与氧元素的原子个数比为 ;
(2)N(NO2)3中氮元素和氧元素的质量比为 ;
(2)N(NO2)3的相对分子质量为 ;
(3)30.4kg的N(NO2)3中含氧元素多少kg?(计算结果精确到0.1%)
答案 分析:
(1)根据N(NO2)3分子的构成进行分析解答.
(2)依据元素的质量比等于各元素相对原子质量和的比分析解答即可.
(3)根据物质的相对分子质量为组成分子的各原子的相对原子质量之和解决;
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:
解:(1)1个N(NO2)3分子是由4个氮原子和6个氧原子,则N(NO2)3中氮元素与氧元素的原子个数比为4:6=2:3.故填:2:3;
(2)依据元素的质量比等于各元素相对原子质量和的比,所以N(NO2)3中氮元素和氧元素的质量比是(14×4):(16×6)=7:12;故填:7:12;
(3)N(NO2)3的相对分子质量为14+(14+16×2)×3=152.故填:152;
(4)30.4kg的N(NO2)3中含氧元素的质量为30.4kg×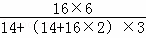 ×100%=19.2kg.故填:19.2kg.
×100%=19.2kg.故填:19.2kg.

小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的,为了了解铬与常见金 属铝、铜在金属活动性顺序中的相对位置关系,他进行如下探究活动。
属铝、铜在金属活动性顺序中的相对位置关系,他进行如下探究活动。
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀 硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液……
硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液……
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr、Al、Cu;②Al、Cr、Cu;③Al、Cu、C r
r
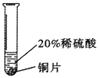
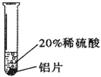
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮后进行下列实验:
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 |
|
|
|
| 实验 现 | 铬片表面产生气泡缓慢,溶液变为 色。 | ____________________ | 铝片表面产生气泡较快。 |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 |
|
| 三种金属在金属活动性顺序中的相对位置关系是__________________________ |
【回答问题】
(1)实验一所发生反应的化学方程式是____________________________。
(2)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是__________。
(3)小清认为只要 选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是________________。
选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是________________。
下图是某钙片的说明书,请阅读解答下列问题。
| X X 钙 片 主要成分:葡萄糖酸钙C6H11O72Ca 药品规格:2.5g每片含C6H11O72Ca 0.2g 用 量:每日2次,每次一片 |
①葡萄糖酸钙中含有_________种元素。
②葡萄糖酸钙中碳与钙的质量比是_______;
③按说明书服用此钙片,每天补充钙的为: 。(只写算式,不算结果)。
友情告知:C6H11O72Ca 的相对分子质量为 430
(2)现有废硫酸 4.9t。废硫酸中 H2SO4 的质量分数为20%与足量的废铁屑反应,可生产FeSO4的质量是多少?
 来立即注入少量澄清石灰水,振荡后发现石灰水 ,通过这两个现象说明酒精燃烧时生成
来立即注入少量澄清石灰水,振荡后发现石灰水 ,通过这两个现象说明酒精燃烧时生成  和 ,该反应的文字表达式为 。
和 ,该反应的文字表达式为 。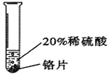


 市被授予中国“文房四宝之乡”,“文房四宝”中的徽墨、宣纸、歙砚是我国享誉中外的文化瑰宝。
市被授予中国“文房四宝之乡”,“文房四宝”中的徽墨、宣纸、歙砚是我国享誉中外的文化瑰宝。