题目内容
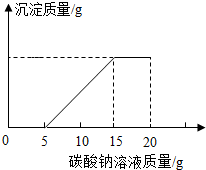 王强同学在完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不含其它的杂质)进行如下实验:取一定量该混合溶液放入烧杯中,再滴入20g溶质质量分数为10.6%的碳酸钠溶液.滴入碳酸钠溶液的质量与生成沉淀的质量的关系如图所示.
王强同学在完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不含其它的杂质)进行如下实验:取一定量该混合溶液放入烧杯中,再滴入20g溶质质量分数为10.6%的碳酸钠溶液.滴入碳酸钠溶液的质量与生成沉淀的质量的关系如图所示.(1)刚加入碳酸钠溶液时,发现没有沉淀生成,却有气泡产生,原因是
(2)计算反应中生成气体的质量.
(3)计算所取混合液中CaCl2的质量.
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:由图中数据可知与混合液中HCl反应、与混合液中氯化钙反应的碳酸钠溶液的质量.
由与混合液中HCl反应的碳酸钠溶液的质量根据碳酸钠与稀盐酸反应的化学方程式可以计算出生成气体的质量.
根据氯化钙与碳酸钠反应的化学方程式可以计算出氯化钙的质量.
由与混合液中HCl反应的碳酸钠溶液的质量根据碳酸钠与稀盐酸反应的化学方程式可以计算出生成气体的质量.
根据氯化钙与碳酸钠反应的化学方程式可以计算出氯化钙的质量.
解答:解:(1)刚加入碳酸钠溶液时,发现没有沉淀生成,却有气泡产生,是碳酸钠与稀盐酸反应生成了氯化钠和水和二氧化碳;
(2)由图中数据可知与HCl反应的碳酸钠溶液的质量为5g.
设生成气体的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
5g×10.6% x
=
,
x=0.22g
(2)由图中数据可知与氯化钙反应的碳酸钠溶液的质量为15g-5g=10g.
设混合液中氯化钙的质量为y.
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111
10g×10.6 y
=
y=1.11g
答案:(1)2HCl+Na2CO3═2NaCl+CO2↑+H2O;
(2)生成气体的质量为0.22g;
(3)混合液中氯化钙的质量为1.11g.
(2)由图中数据可知与HCl反应的碳酸钠溶液的质量为5g.
设生成气体的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
5g×10.6% x
| 106 |
| 5g×10.6% |
| 44 |
| x |
x=0.22g
(2)由图中数据可知与氯化钙反应的碳酸钠溶液的质量为15g-5g=10g.
设混合液中氯化钙的质量为y.
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111
10g×10.6 y
| 106 |
| 10g×10.6% |
| 111 |
| y |
y=1.11g
答案:(1)2HCl+Na2CO3═2NaCl+CO2↑+H2O;
(2)生成气体的质量为0.22g;
(3)混合液中氯化钙的质量为1.11g.
点评:本题主要考查有关化学方程式的计算和溶质质量分数的计算,难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、天然水经自来水厂净化处理后就得到了纯净水 |
| B、明矾净化水的作用是消毒杀菌 |
| C、生活中降低水的硬度的方法是蒸馏 |
| D、检验硬水和软水的简便方法是加肥皂水 |
有氢气和氧气的混合物20g,点燃使其完全燃烧反应,当冷却至室温后,测得生成18g水,问原混合气体中氢气和氧气的质量比( )
| A、1:9 或2:3 |
| B、2:3 或1:4 |
| C、1:9或1:4 |
| D、1:4或1:8 |
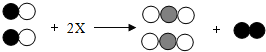
如图为氧化汞受热分解时的微观过程示意图,由此得出的下列信息不正确的是( )

| A、反应前后,原子的数目不变 |
| B、该反应过程中,原子发生了重新组合 |
| C、反应过程中,原子是最小的粒子 |
| D、反应前后,分子的种类不变 |
2007年3月15日某报纸报道,某品牌妙芙欧式蛋糕中铝的含量超出GB2762-2005标准多倍.这里的“铝”是指( )
| A、铝单质 | B、铝元素 |
| C、铝分子 | D、铝原子 |
下列对相关实验现象的描述错误的是( )
| A、木炭在氧气中燃烧发出白光 |
| B、把铁钉放入硫酸铜溶液中,铁钉的表面有铜生成 |
| C、硫在空气中燃烧发出淡蓝色火焰 |
| D、红磷在空气中燃烧产生大量白烟 |
学习科学知识可以用来辨别“真”、“伪”,通过分析下列叙述属于“真”的是( )
| A、绿色食品是不含任何化学物质的食品 |
| B、为延长灯泡的使用寿命,可在灯泡中充入氮气 |
| C、青少年缺钙会得佝偻病和发育不良,因此需要经常补充钙单质 |
| D、有人称自己有特异功能,能将普通的铜、铝转变成黄金 |
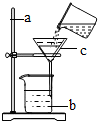 如图是某同学做“净化黄泥水”实验时的过滤装置图,请完成以下空白:
如图是某同学做“净化黄泥水”实验时的过滤装置图,请完成以下空白:
 .
.