题目内容
4.某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如表:| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
| 68.0 | 0.1 | 66.5 |
(1)过氧化氢中,氢元素与氧元素的质量之比为1:16.
(1)该同学制得氧气的质量为1.6g.
(2)该同学所用过氧化氢溶液的溶质质量分数.
分析 根据过氧化氢的化学式可以计算氢元素和氧元素质量比;
过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气质量可以计算过氧化氢质量,进一步可以计算所用过氧化氢溶液的溶质质量分数.
解答 解:(1)过氧化氢中,氢元素与氧元素的质量之比为(1×2):(16×2)=1:16.
故填:1:16.
(1)该同学制得氧气的质量为:68.0g+0.1g-66.5g=1.6g.
故填:1.6g.
(2)设过氧化氢质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x 1.6g
$\frac{68}{x}$=$\frac{32}{1.6g}$,
x=3.4g,
该同学所用过氧化氢溶液的溶质质量分数为:$\frac{3.4g}{68.0g}$×100%=5%,
答:该同学所用过氧化氢溶液的溶质质量分数为5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
15.下列说法正确的是( )
| A. | 浓溶液不一定是饱和溶液 | B. | 浓溶液一定是饱和溶液 | ||
| C. | 稀溶液一定比浓溶液含有较少溶质 | D. | 稀溶液一定是不饱和溶液 |
12.二氧化硅是由硅、氧等因素组成,这两种元素的本质区别是( )
| A. | 电子数不同 | B. | 质子数不同 | ||
| C. | 中子数不同 | D. | 相对原子质量不同 |
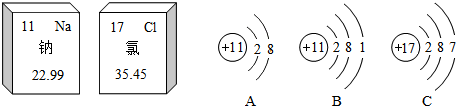
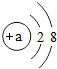 ,当a=9时,该粒子是阴离子(填“原子”、“阳离子”、或“阴离子”).该元素的化学性质与上面哪种元素的化学性质最相似?C(填序号),它属于非金属元素(填“金属“或“非金属“),当a=10时,该粒子是原子.
,当a=9时,该粒子是阴离子(填“原子”、“阳离子”、或“阴离子”).该元素的化学性质与上面哪种元素的化学性质最相似?C(填序号),它属于非金属元素(填“金属“或“非金属“),当a=10时,该粒子是原子.