题目内容
7.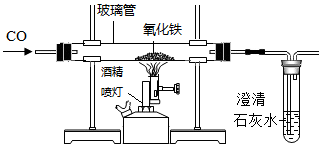 在实验室里可以利用如图装置制得铁.
在实验室里可以利用如图装置制得铁.(1)实验过程中,玻璃管内可以观察到的现象是红色粉末慢慢变成黑色,发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)实验结束时,要继续通入一氧化碳,直到玻璃管冷却,这是为了防止铁被重新氧化,石灰水倒吸炸裂玻璃管.
(3)此实验装置的不足之处是缺少尾气处理装置.
分析 (1)氧化铁在高温的条件下被一氧化碳还原为铁,同时生成二氧化碳;
(2)根据实验步骤和注意事项分析,避免还原出来的铁再次被氧化;
(3)根据尾气中含有一氧化碳会污染空气考虑.
解答 解:(1)氧化铁与一氧化碳在高温条件下生成铁和二氧化碳,观察到玻璃管内的红色粉末慢慢变成黑色;故答案为:红色粉末慢慢变成黑色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)若先停止通一氧化碳,再停止加热,会使石灰水倒吸到玻璃管内,使试管炸裂,刚还原出来的铁也会再次被氧化,所以实验结束后要继续通入一氧化碳直到装置冷却,故填:防止铁被重新氧化,石灰水倒吸炸裂玻璃管;
(3)尾气中可能有一氧化碳,一氧化碳有毒,所以一定要进行尾气处理,该装置缺少尾气处理装置;故填:缺少尾气处理装置.
点评 本题通过一氧化碳还原氧化铁考查常见物质的性质,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
17.准晶体可能具有下列性质,其中属于化学性质的是( )
| A. | 密度低 | B. | 抗氧化性强 | C. | 导电性差 | D. | 耐磨损 |
18.某化学兴趣小组在探究硫酸和氢氧化钡与稀盐酸中和反应实验时,滴加酚酞溶液作为指示剂,当溶液由红色变为无色时,同学们决定对反应后溶液中溶质的成分进行探究.
【提出问题】反应后溶液中的溶质是什么?
【做出猜想】猜想一:水;猜想二:氢氧化钡; 猜想三:硫酸.
请将猜想三补充完整,并说出你猜想的理由是硫酸过量时,溶质是硫酸.验证正确的猜想,过程如下
【拓展与应用】举例说明中和反应在日常生活和工农业生产中的应用熟石灰中和酸性土壤(答一点)
【提出问题】反应后溶液中的溶质是什么?
【做出猜想】猜想一:水;猜想二:氢氧化钡; 猜想三:硫酸.
请将猜想三补充完整,并说出你猜想的理由是硫酸过量时,溶质是硫酸.验证正确的猜想,过程如下
| 实验操作 | 实验现象 | 实验结论 |
15.把下列物质溶于水中,一定能得到无色溶液的是( )
| A. | NaOH、MgSO4、CaCl2、HNO3 | B. | HNO3、BaCl2、AgNO3、KOH | ||
| C. | KMnO4、NaNO3、HCl、MgSO4 | D. | KNO3、Na2CO3、H2SO4、NaOH |
12.下列各项:①原子的数目;②分子的数目;③元素的种类;④物质的种类;⑤物质的分子个数;⑥各种原子的总数.在化学反应前后,肯定没有变化的是( )
| A. | ①②③⑤ | B. | ①⑥ | C. | ①③⑥ | D. | ②③⑤ |
19.常温下,碘与镁化合时速率很慢,若滴入几滴水,则反应相当剧烈,形成一股美丽的紫色烟雾,这里水所起的作用是( )
| A. | 反应物 | B. | 氧化剂 | C. | 催化剂 | D. | 生成物 |
17.化学式的学习具有重要意义,在O2、CO2、H2O2三种物质的分子中都含有( )
| A. | 氧分子 | B. | 1个氧分子 | C. | 氧原子 | D. | 2个氧元素 |