题目内容
 请根据如图所示的实验过程和提供的数据,计算生石灰样品中钙元素的质量.(不考虑其它因素对实验的影响)
请根据如图所示的实验过程和提供的数据,计算生石灰样品中钙元素的质量.(不考虑其它因素对实验的影响)考点:根据化学反应方程式的计算,化合物中某元素的质量计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:反应前后的质量差即为反应生成二氧化碳的质量;
根据二氧化碳的质量可以计算碳酸钙的质量,根据碳酸钙的质量可以计算氧化钙的质量,进一步可以计算生石灰样品中钙元素的质量.
根据二氧化碳的质量可以计算碳酸钙的质量,根据碳酸钙的质量可以计算氧化钙的质量,进一步可以计算生石灰样品中钙元素的质量.
解答:解:生成二氧化碳的质量为:33g+250g-280.8g=2.2g.
设:碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2 g
=
,
x=5g,
样品中氧化钙的质量为:33g-5g=28g,
碳酸钙中钙元素的质量为:5g×
×100%=2g,
氧化钙中钙元素质量为:28g×
×100%=20g,
生石灰样品中钙元素的质量为:2g+20g=22g,
答:生石灰样品中钙元素的质量为22g.
设:碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2 g
| 100 |
| x |
| 44 |
| 2.2g |
x=5g,
样品中氧化钙的质量为:33g-5g=28g,
碳酸钙中钙元素的质量为:5g×
| 40 |
| 100 |
氧化钙中钙元素质量为:28g×
| 40 |
| 56 |
生石灰样品中钙元素的质量为:2g+20g=22g,
答:生石灰样品中钙元素的质量为22g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
实验室可用氯酸钾、高锰酸钾和过氧化氢溶液制取氧.下列有关说法正确的是( )
| A、三个反应均需加入二氧化锰作催化剂 |
| B、三种方法的发生装置都相同 |
| C、三种方法都可以用试管做反应容器 |
| D、三种方法制得氧气的质量均等于参加反应的反应物中氧元素的质量 |
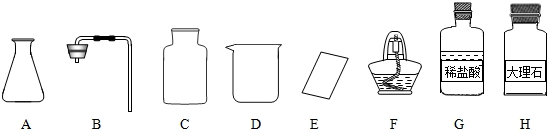
 热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算:
热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算:
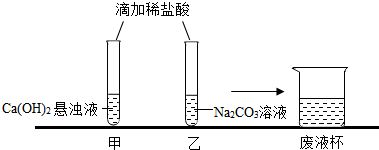
 如图所示,A、B、C、D、E、F均是初中化学常见物质.A与B发生的是复分解反应,B与C发生的是中和反应,气体D可使澄清石灰水变浑浊,F是配制生理盐水和腌渍食品的盐.结合图中信息,回答有关问题:
如图所示,A、B、C、D、E、F均是初中化学常见物质.A与B发生的是复分解反应,B与C发生的是中和反应,气体D可使澄清石灰水变浑浊,F是配制生理盐水和腌渍食品的盐.结合图中信息,回答有关问题: