题目内容
11.A、B、C、D、E 初中化学常见的物质.B是一种氧化物,相对分子质量为44,B中两元素质量比为3:8;人体胃酸中含有D,可帮助消化;生活中F是一种最常见的溶剂,且F和G的组成元素相同;A和E都是由三种元素组成的化合物.它们之间的一部分关系如图所示,(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.部分反应物或生成物已略去)请回答下列问题:
(1)D物质的化学式为HCl;F物质的化学式为H2O.
(2)G→C反应的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)A与D反应的化学反应方程式为HCl+NaOH=NaCl+H2O,该反应放出(填“放出”或“吸收”)热量.
(4)写出C物质的一种用途:医疗急救、炼钢等.
分析 根据A、B、C、D、E 初中化学常见的物质,B是一种氧化物,相对分子质量为44,B中两元素质量比为3:8,所以B是二氧化碳,人体胃酸中含有D,可帮助消化,所以D是盐酸,生活中F是一种最常见的溶剂,所以F是水,F和G的组成元素相同,G会转化成F,所以G是双氧水;双氧水分解可以生成水和氧气,所以C是氧气,A和E都是由三种元素组成的化合物,E和二氧化碳可以互相转化,所以E可以是碳酸钠,A和碳酸钠也可以相互转化,所以A是氢氧化钠,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E 初中化学常见的物质,B是一种氧化物,相对分子质量为44,B中两元素质量比为3:8,所以B是二氧化碳,人体胃酸中含有D,可帮助消化,所以D是盐酸,生活中F是一种最常见的溶剂,所以F是水,F和G的组成元素相同,G会转化成F,所以G是双氧水;双氧水分解可以生成水和氧气,所以C是氧气,A和E都是由三种元素组成的化合物,E和二氧化碳可以互相转化,所以E可以是碳酸钠,A和碳酸钠也可以相互转化,所以A是氢氧化钠,经过验证,推导正确,所以D是HCl,F是H2O;
(2)G→C的反应是过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)A与D的反应是氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:HCl+NaOH=NaCl+H2O,该反应放出热量;
(4)C是氧气,能够支持燃烧和呼吸,常用于医疗急救、炼钢等.
故答案为:(1)HCl,H2O;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)HCl+NaOH=NaCl+H2O,放出;
(4)医疗急救、炼钢等.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 阅读快车系列答案
阅读快车系列答案 某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:①称取1.6 g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按如表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果作比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影Ⅱ向实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | ||
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
(1)上述实验步骤中需要使用玻璃棒的是①②③(填序号).
(2)表格中的“待测数据”是指生成50mL气体所需要的时间.
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意ad(填字母编号).
a.视线与凹液面最低处相平
b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管内液面相平再读数
(4)若50 mL量气管中液面的位置如图乙所示,A与B 刻度间相差1 mL,刻度A为20,则此时气体体积的读数为20.8.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.(提示:可从催化剂的概念完 成实验)
| 实验步骤 | 设计这一步骤的目的 |
| 以上实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| A. | 手持试管,应垂直拿稳 | |
| B. | 手拿试剂瓶,标签向外,以防腐蚀标签 | |
| C. | 试剂瓶口不要紧贴试管口,以防污染 | |
| D. | 把试剂瓶塞拿下,倒放在桌面,用完立即将瓶塞盖上 |
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
不选择第③组药品的原因是反应速度太快不利于收集.
(2)选择装置.他选择图中B作为制取的发生装置.你认为他选择的依据是固体和液体发生反应,反应条件是常温,小丽认为利用B装置也可以选择第③组药品来制取二氧化碳,理由是利用分液漏斗控制液体流速,可以控制反应速度.

(3)制取气体.将药品装入所选装置制取气体,并只能用图中D组装置收集.原因是二氧化碳能溶于水,密度比空气大.
(4)气体检验.小明将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?不正确请说明理由.因为还有其他气体也可以使紫色石蕊变红色.请写出正确的检验二氧化碳的方法:Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).

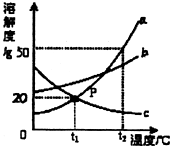 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题: