题目内容
14.某校化学兴趣小组就空气中氧气的含量进行实验探究.【设计实验】
第一小组同学共同设计了如图所示的A、B两套装置.

(1)红磷在瓶内燃烧时的现象是产生大量的白烟,放出大量的热,生成一种白色固体;
(2)为了保证结果的准确,第一小组同学在实验过程中等集气瓶冷却至室温后才打开止水夹,这样操作的原因是更准确地得到氧气的含量.
(3)集气瓶中倒吸的水少于$\frac{1}{5}$的原因红磷量不足;(任写一条)
【改进实验】
第二小组同学查阅资料得知:当温度达到40℃时白磷就能在空气中燃烧.五氧化二磷会刺激人的呼吸道,影响健康.于是他们将试管的容积分成五等分,做好标记.在试管中加入一小块(足量)白磷,用橡皮塞塞紧试管口,将试管放入热水中,使白磷燃烧.待白磷熄灭并冷却到室温后,将试管倒立于盛有室温下水的水槽中(如图B),并在水中将橡皮塞取下.
(1)此装置的优点是(任写一点)测定结果更准确,能够减少空气污染;
(2)实验结束后水倒吸进入试管约占试管体积的$\frac{1}{5}$,本实验还能够得到氮气的有关性质,请写出两点:不溶于水,不能燃烧,也不能支持燃烧.
分析 【设计实验】
(1)根据红磷燃烧的现象进行分析解答即可.
(2)如果温度高于室温,则进入集气瓶中的水会不到集气瓶容积的五分之一,使测定结果不准确;
(3)产生误差的原因可以从装置的气密性、药品的用量、装置是否冷却等方面进行评价.
【改进实验】
(1)利用改进后的装置进行实验,能够避免燃烧匙进入集气瓶时空气向外扩散,同时能够防止生成的五氧化二磷向外扩散;
(2)氮气不溶于水,不能燃烧,不支持燃烧.
解答 解:【设计实验】
(1)红磷在氧气中燃烧,产生大量的白烟,放出大量的热,生成一种白色固体.
故填:产生大量的白烟,放出大量的热,生成一种白色固体.
(2)在实验过程中等集气瓶冷却至室温后才打开止水夹,这样操作的原因是:更准确地得到氧气的含量.
故填:更准确地得到氧气的含量.
(3)若红磷的量不足,导致不能将装置内的氧气完全反应掉,因此测得氧气的体积分数小于五分之一;
若装置漏气,导致空气进入集气瓶内,因此测得的氧气的体积分数小于五分之一;
若未等到装置冷却到室温,就打开止水夹,会使集气瓶内的气体处于膨胀状态,因此测得的氧气体积分数会小于五分之一.
故答案为:红磷量不足;未等到冷却到室温就打开止水夹等.
【改进实验】
(1)此装置的优点是:能使测定结果更准确,能够减少空气污染.
故填:测定结果更准确,能够减少空气污染.
(2)本实验能够得到该结论主要是运用了氮气的性质有:氮气不溶于水,不能燃烧,不支持燃烧.
故填:不溶于水;不能燃烧,也不能支持燃烧.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
2.化学上把“生成新物质的变化叫做化学变化”,下面对化学变化中“新物质”正确的是( )
| A. | “新物质”自然界中不存在的物质 | |
| B. | “新物质”就是与变化前的物质颜色、状态等方面有所不同的物质 | |
| C. | 凡是变化过程中有明显现象产生,说明此变化过程中一定有“新物质”生成 | |
| D. | “新物质”就是与变化前的物质在组成结构上不同的物质 |
9.室温下,向一定质氯化钠溶液中加入10g氯化钠固体,充分搅拌后,尚有部分固体未溶解,加入10g水后,固体全部溶解.下列判断正确的是( )
| A. | 加水前一定是饱和溶液 | B. | 加氯化钠前可能是饱和溶液 | ||
| C. | 加水后一定是饱和溶液 | D. | 加水后一定是不饱和溶液 |
19.如图是某化学反应的微观示意图,你认为下列说法不正确的是( )
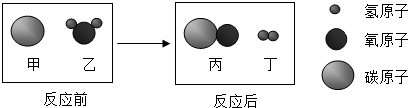

| A. | 反应前后各元素的化合价都发生了改变 | |
| B. | 该反应是置换反应 | |
| C. | 乙、丙两种物质都是氧化物 | |
| D. | 反应前后原子的种类、数目都不变 |
4.某城市有甲、乙两工厂排放污水,污水中各含有下列6种离子中的3种(两厂不含相同离子):Ag+、Ba2+、Na+、Cl-、CO32-、NO3-.若两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便会变成无色澄清只含硝酸钠的液体,污染程度会大大降低.关于污染源的分析,你认为正确的是( )
| A. | Cl-和NO3-一定不在同一工厂 | B. | Na+和NO3-来自同一工厂 | ||
| C. | Ag+和Na+可能在同一工厂 | D. | CO32-和NO3-可能来自同一工厂 |
