题目内容
4.荔枝肉产鲜时半透明凝脂状,味香美,广受人们的喜爱.荔枝因含有机物异戊酸异戊酯(化学式为C10H20O2)而具有芳香味.试计算:(1)异戊酸异戊酯中碳、氢、氧元素的质量比.
(2)异戊酸异戊酯中氢元素的质量分数(计算结果保留一位小数)
(3)如果100g异戊酸异戊酯中氢元素全部转化生成水,则可以生成水多少克.
分析 (1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答本题;
(2)根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{该物质相对分子质量}$×100% 进行解答本题;
(3)根据水中氢元素的质量与100g异戊酸异戊酯中氢元素相等的关系进行分析解答本题.
解答 解:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,则异戊酸异戊酯中碳、氢、氧元素的质量比为:(12×10):(1×20):(16×2)=30:5:8; 故答案为:30:5:8;
(2)根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{该物质相对分子质量}$×100%,
则异戊酸异戊酯中氢元素的质量分数=$\frac{20}{172}$×100%=11.6%,故答案为:11.6%;
(3)设 x 水中氢元素的质量与100g异戊酸异戊酯中氢元素相等,则有:x×$\frac{2}{18}$×100%=100×11.6%,解答 x=104.4 g;
故答案为:
(1)30:5:8;(2)11.6%;(3)104.4 g;
点评 本题主要考查学生根据化合物中各元素质量比,物质中某元素的质量分数进行分析解题的能力,必须掌握有关质量分数的计算.

练习册系列答案
相关题目
14.从100克10%的NaCl溶液中取出10克,那么剩下的90克NaCl的溶液中溶质质量分数是( )
| A. | 1% | B. | 90% | C. | 10% | D. | 11.1% |
15.下列实验现象中描述正确的是( )
| A. | 镁条燃烧发出耀眼的强光,生成白色的氧化镁 | |
| B. | 红磷在氧气中剧烈燃烧,产生大量的白雾 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰 | |
| D. | 水电解时生成的氧气和氢气的体积比约为1:2 |
16.造成空气污染的主要污染物是( )
| A. | 二氧化硫、二氧化氮、二氧化碳 | B. | 二氧化硫、二氧化氮、一氧化碳 | ||
| C. | 二氧化硫、一氧化碳、氢气 | D. | 二氧化氮、一氧化碳、水蒸气 |
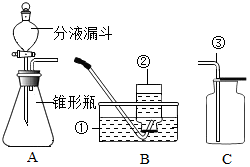 常温下,过氧化氢(H2O2)溶液在二氧化锰的催化作用下能迅速分解生成氧气和水.现有如图所示的实验装置(分液漏斗可以通过调节活塞控制液体的流速)现用5%过氧化氢溶液制取氧气,请回答有关问题.
常温下,过氧化氢(H2O2)溶液在二氧化锰的催化作用下能迅速分解生成氧气和水.现有如图所示的实验装置(分液漏斗可以通过调节活塞控制液体的流速)现用5%过氧化氢溶液制取氧气,请回答有关问题.