题目内容
盐酸和硫酸是化学工业的重要产品和原料,也是我们实验室常用的化学试剂.
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性.
(2)写出稀盐酸与下列物质反应的化学方程式:
①与锌粒反应:
②与碳酸钠溶液反应:
③与硝酸银溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)
(3)硫酸的下列用途中,可以用盐酸代替硫酸的是 (填编号)
①金属表面除锈 ②制造化肥(NH4)2SO4 ③处理碱性废水 ④制造胆矾
(4)某同学为鉴定某一无色溶液是否为稀硫酸,进行了以下实验:
步骤一:取少量溶液于试管中,滴加石蕊试液,溶液变红色,表明溶液中一定有氢离子;
步骤二:另取少量溶液于试管中, ,证明溶液中一定有硫酸根离子,最终确定该溶液为硫酸.
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有
(2)写出稀盐酸与下列物质反应的化学方程式:
①与锌粒反应:
②与碳酸钠溶液反应:
③与硝酸银溶液反应:
上述反应中,属于酸的共同性质的是
(3)硫酸的下列用途中,可以用盐酸代替硫酸的是
①金属表面除锈 ②制造化肥(NH4)2SO4 ③处理碱性废水 ④制造胆矾
(4)某同学为鉴定某一无色溶液是否为稀硫酸,进行了以下实验:
步骤一:取少量溶液于试管中,滴加石蕊试液,溶液变红色,表明溶液中一定有氢离子;
步骤二:另取少量溶液于试管中,
考点:酸的化学性质,浓硫酸的性质及浓硫酸的稀释,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)根据浓硫酸具有强烈的腐蚀性进行分析解答.
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.考虑酸的共同性质进行回答.
(3)盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应;酸碱进行中和反应.
(4)判断某一无色溶液是否为稀硫酸,就需要验证溶液中是否含有氢离子和硫酸根离子,从提供的信息可知①②均能验证溶液中含有氢离子,③和④的差别在于对实验产生的白色沉淀是否进行了验证,由所学可知这种情况下只有白色沉淀不溶于硝酸才可以证明该白色沉淀是硫酸钡,据此分析即可.
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.考虑酸的共同性质进行回答.
(3)盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应;酸碱进行中和反应.
(4)判断某一无色溶液是否为稀硫酸,就需要验证溶液中是否含有氢离子和硫酸根离子,从提供的信息可知①②均能验证溶液中含有氢离子,③和④的差别在于对实验产生的白色沉淀是否进行了验证,由所学可知这种情况下只有白色沉淀不溶于硝酸才可以证明该白色沉淀是硫酸钡,据此分析即可.
解答:解:
(1)浓硫酸具有吸水性,在实验室常用作干燥剂.
(2)①锌与盐酸反应生成氯化锌和氢气,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
②碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
③硝酸银与盐酸反应生成氯化银沉淀和硝酸,反应的化学方程式为:HCl+AgNO3═HNO3+AgCl↓.
酸的共同性质有:可以和指示剂发生显色反应,可以和活泼金属反应,可以和碱反应生成盐和水,可以和碱性氧化物反应生成盐和水,可以和部分盐反应生成新酸和新盐等.
故选:①②;
(3)①盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应,都能用于金属表面除锈,故选项正确.
②制造化肥(NH4)2SO4,盐酸不含硫元素,故不能用盐酸代替硫酸,故选项错误.
③利用酸碱中和反应,处理碱性废水,故能用盐酸代替硫酸,故选项正确.
④胆矾为5水硫酸铜,而盐酸不含硫元素,故不能制造胆矾,不能用盐酸代替硫酸,故选项错误.
故选:①③;
(4)为鉴定某一无色溶液是否为稀硫酸:取少量溶液于试管中,滴加石蕊试液,溶液变红色,说明溶液呈酸性;取少量溶液于试管中,滴加硝酸钡溶液,振荡,有白色沉淀生成,滴加稀硝酸,沉淀不溶解,说明该白色沉淀是硫酸钡,从而可证明溶液中一定有硫酸根离子.
故答案为:
(1)吸水;
(2)①Zn+2HCl═ZnCl2+H2↑.
②Na2CO3+2HCl═2NaCl+H2O+CO2↑.
③HCl+AgNO3═HNO3+AgCl↓; ①②;
(3)①③;
(4)滴加硝酸钡溶液,振荡,有白色沉淀生成,滴加稀硝酸,沉淀不溶解,
(1)浓硫酸具有吸水性,在实验室常用作干燥剂.
(2)①锌与盐酸反应生成氯化锌和氢气,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
②碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
③硝酸银与盐酸反应生成氯化银沉淀和硝酸,反应的化学方程式为:HCl+AgNO3═HNO3+AgCl↓.
酸的共同性质有:可以和指示剂发生显色反应,可以和活泼金属反应,可以和碱反应生成盐和水,可以和碱性氧化物反应生成盐和水,可以和部分盐反应生成新酸和新盐等.
故选:①②;
(3)①盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应,都能用于金属表面除锈,故选项正确.
②制造化肥(NH4)2SO4,盐酸不含硫元素,故不能用盐酸代替硫酸,故选项错误.
③利用酸碱中和反应,处理碱性废水,故能用盐酸代替硫酸,故选项正确.
④胆矾为5水硫酸铜,而盐酸不含硫元素,故不能制造胆矾,不能用盐酸代替硫酸,故选项错误.
故选:①③;
(4)为鉴定某一无色溶液是否为稀硫酸:取少量溶液于试管中,滴加石蕊试液,溶液变红色,说明溶液呈酸性;取少量溶液于试管中,滴加硝酸钡溶液,振荡,有白色沉淀生成,滴加稀硝酸,沉淀不溶解,说明该白色沉淀是硫酸钡,从而可证明溶液中一定有硫酸根离子.
故答案为:
(1)吸水;
(2)①Zn+2HCl═ZnCl2+H2↑.
②Na2CO3+2HCl═2NaCl+H2O+CO2↑.
③HCl+AgNO3═HNO3+AgCl↓; ①②;
(3)①③;
(4)滴加硝酸钡溶液,振荡,有白色沉淀生成,滴加稀硝酸,沉淀不溶解,
点评:本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)、酸的用途等并能灵活运用是正确解答本题的关键.掌握氢离子与硫酸根离子的鉴定.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
小芳阅读课外书籍得知,SO2+Ca (OH)2=CaSO3↓ (白色)+H2O,SO2+H2O=H2SO3(弱酸)从而获得以下结论,其中错误的是( )
| A、能使澄清石灰水变浑浊的气体不一定是二氧化碳 |
| B、能使紫色石蕊溶液变红的气体不一定是二氧化碳 |
| C、可用排水集气法收集二氧化硫 |
| D、可用闻气味法鉴别二氧化碳和二氧化硫 |
世界上每年有上万家庭发生火灾,造成了极大损失,如果掌握一些安全知识和紧急灭火措施,就能避免火灾.下列说法你认为正确的是( )
| A、用打火机点火检查液化气罐是否漏气 |
| B、油锅着火用锅盖盖灭 |
| C、电器着火用水扑灭 |
| D、室内着火时打开门窗通风 |
下列实验操作中,错误的是( )
A、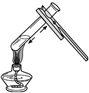 给液体加热 |
B、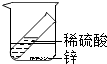 验证质量守恒定律 |
C、 读取液体体积 |
D、 检查装置的气密性 |
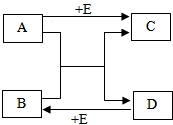 已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如下图所示.如果已知A和B均为黑色固体,C是造成温室效应的主要气体,D是一种亮红色的金属单质.则回答:
已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如下图所示.如果已知A和B均为黑色固体,C是造成温室效应的主要气体,D是一种亮红色的金属单质.则回答:
 生活中处处有化学.
生活中处处有化学.