题目内容
现有11.6g含少量杂质氯化钠的碳酸钠,与100g稀盐酸恰好完全反应生成4.4g二氧化碳.求:
(1)样品中碳酸钠的质量分数.
(2)反应后的溶液中溶质的质量分数.(计算结果保留到0.1%).
(1)样品中碳酸钠的质量分数.
(2)反应后的溶液中溶质的质量分数.(计算结果保留到0.1%).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑和生成二氧化碳的质量可以计算出样品中Na2CO3的质量,进而求出该纯碱样品中Na2CO3的质量分数;
(2)反应后所得溶液为氯化钠溶液,而样品中的氯化钠不与盐酸反应;至完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠,据此解答即可.
(2)反应后所得溶液为氯化钠溶液,而样品中的氯化钠不与盐酸反应;至完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠,据此解答即可.
解答:解:设样品中碳酸钠的质量为x,生成氯化钠的质量为y,则
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
=
=
x=10.6g,y=11.7g
(1)样品中碳酸钠的质量分数:
×100%=91.4%;
(2)所得溶液中NaCl的质量为原样品中氯化钠的质量与生成氯化钠的质量之和.
氯化钠的质量=11.7g+(11.6g-10.6g)=12.7g
所得溶液的溶质质量分数:
×100%=11.8%
答:样品中碳酸钠的质量分数为91.4%,所得溶液的溶质质量分数为11.8%.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
| 106 |
| x |
| 117 |
| y |
| 44 |
| 4.4g |
x=10.6g,y=11.7g
(1)样品中碳酸钠的质量分数:
| 10.6g |
| 11.6g |
(2)所得溶液中NaCl的质量为原样品中氯化钠的质量与生成氯化钠的质量之和.
氯化钠的质量=11.7g+(11.6g-10.6g)=12.7g
所得溶液的溶质质量分数:
| 12.7g |
| 11.6g+100g-4.4g |
答:样品中碳酸钠的质量分数为91.4%,所得溶液的溶质质量分数为11.8%.
点评:要想解答好这类题目,要理解和熟记根据化学反应方程式的计算步骤、格式以及与之相关的知识等,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
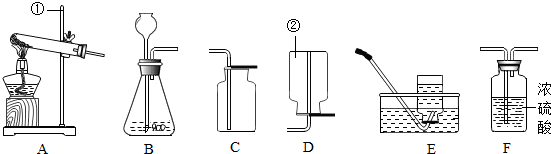
按如图所示装置进行实验,不能达到对应目的是( )
A、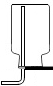 收集H2 |
B、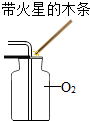 验满O2 |
C、 配制20%的溶液 |
D、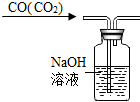 除去CO2 |
工业上用氨气(NH3)制取硝酸(HNO3),工业流程中核心化学反应依次为:①4NH3+5O2
4NO+6H2O ②2NO+O2=2NO2③3NO2+H2O=2HNO3+NO,下列判断不正确的是( )
| ||
| A、①为置换反应 |
| B、上述含氮物质中氮元素的化合价有-3,+2,+4,+5 |
| C、通常情况下一氧化氨不与水反应 |
| D、制取硝酸过程中产生的NO应循环使用 |
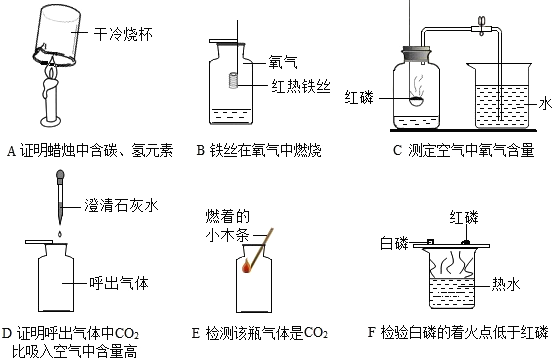
 向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如图所示.
向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如图所示.