题目内容
4.我国海岸线长达3.2万千米,海洋专属经济区幅员辽阔,海洋资源丰富,开发前景十分远大.(1 )我国海盐年产量3千多万吨,居世界第一位.目前从海水中提取食盐的方法主要为:
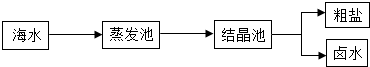
一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会不变(填“增大”、“不变”或|减小“).
(2)金属铁广泛应用于生活、生产和国防工业,从卤水中提取镁的过程如图所示:

在上述转化过程中:①处所发生的反应属于复分解反应(填”中和“”复分解“”氧化“”化合“”分解“之一)
(3)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,KCl和KNO3的溶解度曲线如图所示,试回答下列问题:
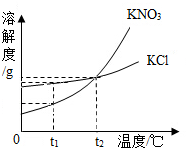
①t1℃时,KCl饱和溶液的溶质的质量分数大于KNO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)
②t2℃时KCl和KNO3的溶解度曲线交于一点,该点表示的意义为t2℃时,氯化钾和硝酸钾两物质的溶解度相等.
③若KNO3中混有少量KCl,可采用降温结晶的方法提纯KNO3.
④已知20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g,在20℃时,向盛有100g水的烧杯中加入40gKNO3‘充分溶解,得到该温度时KNO3的(填“饱和”“不饱和”之一)溶液.若使烧杯内物质缓慢升温至40℃,在该温度下,最后所得溶液中溶质与溶剂的质量之比为2:5(填最简整数比).
分析 (1)根据在蒸发池中,水蒸发了,溶剂的质量减少,溶质的质量不变进行分析;
(2)根据①处发生的反应是氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙进行分析;
(3)根据氯化钾和硝酸钾的溶解度曲线进行分析;
运用溶解度曲线上的交点是该温度下物质的溶解度相等解答;
根据物质的溶解度受温度的影响情况来分析;
根据20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g进行分析.
解答 解:(1)在蒸发池中,水蒸发了,溶剂的质量减少,溶质的质量不变;故填:不变;
(2)①处发生的反应是氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,属于复分解反应;故填:复分解;
(3)①通过分析溶解度曲线,可以看出,t1℃时,氯化钾的溶解度大于硝酸钾的溶解度,所以KCl饱和溶液的溶质质量分数大于KNO3饱和溶液的溶质质量分数;
故填:大于;
②t2℃时,氯化钾和硝酸钾两物质的溶解度曲线相交,说明该温度下二者的溶解度相等,故答案:t2℃时,氯化钾和硝酸钾两物质的溶解度相等;
③KNO3的溶解度受度变化影响较大,KCl的溶解度受温度影响较小,所以若KNO3中混有少量KCl,可利用降温结晶的方法提纯KNO3;故填:降温结晶;
④20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g,在20℃时,向盛有200g水的烧杯中加入80gKNO3,溶解的硝酸钾为63.2g,所以得到该温度时KNO3的饱和溶液,若使烧杯内物质缓慢升温至80℃,在该温度下,固体全部溶解,所以最后所得溶液中溶质与溶剂的质量之比为80g:200g=2:5.
故填:饱和;2:5.
点评 本题考查了据溶解度曲线的意义和饱和溶液中溶质的质量分数分析解答问题,难度不大.

练习册系列答案
相关题目
10.氢元素有3种不同的原子,其原子核内的中子数依次为0、1、2.这3种原子与金属锂形成的氢化锂“三兄弟”-LiH、LiD、LiT是“神舟七号”的燃料.下列说法正确的是( )
| A. | H、D、T相对原子质量之比为1:2:3 | |
| B. | LiH、LiD、LiT相对分子质量相同 | |
| C. | H、D、T化学性质不同 | |
| D. | LiH、LiD、LiT中Li元素质量分数相等 |
7.下列物质中不能鉴别NaCl、Ca(OH)2、稀盐酸三种溶液的是( )
| A. | 酚酞溶液 | B. | 紫色石蕊溶液 | C. | 稀硫酸 | D. | 碳酸钠溶液 |
14.下列物质中,属于酸式盐的是( )
| A. | Fe2O3 | B. | Na2SO4 | C. | NaHCO3 | D. | Cu2(OH)2CO3 |
16.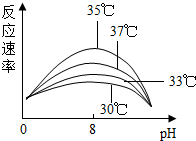 某同学研究温度和pH对某酶反应催化作用速率的影响,得到如图的曲线.下列分析正确的是( )
某同学研究温度和pH对某酶反应催化作用速率的影响,得到如图的曲线.下列分析正确的是( )
 某同学研究温度和pH对某酶反应催化作用速率的影响,得到如图的曲线.下列分析正确的是( )
某同学研究温度和pH对某酶反应催化作用速率的影响,得到如图的曲线.下列分析正确的是( )| A. | 该酶催化反应的最适温度为35℃左右,最适pH为8 | |
| B. | 当pH为8时,影响反应速率的主要因素是底物浓度和酶浓度 | |
| C. | 随pH升高,该酶催化反应的最适温度也逐渐升高 | |
| D. | 当pH为任何一固定值时,实验结果都可以证明温度对反应速率的影响 |
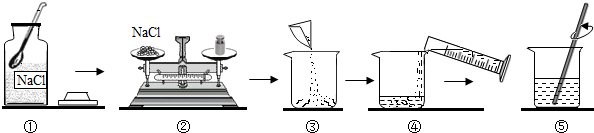
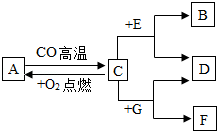 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系: