题目内容
(1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,再逐滴向锥形瓶中滴人稀硫酸并振荡,观察到的现象是 ,溶液的pH (填“增大”或“减小”).
(2)有一瓶溶液pH是4.5,如果要使溶液的pH升高,可以用 的方法.
(2)有一瓶溶液pH是4.5,如果要使溶液的pH升高,可以用
考点:中和反应及其应用,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:(1)氢氧化钠溶液呈碱性,滴加酚酞溶液变红,与稀硫酸发生中和反应而导致溶液OH-离子浓度减小,以此分析;
(2)显酸性的溶液加水稀释时溶液的pH升高,加入显碱性的物质时溶液的pH也升高.
(2)显酸性的溶液加水稀释时溶液的pH升高,加入显碱性的物质时溶液的pH也升高.
解答:解:(1)氢氧化钠溶液呈碱性,能使酚酞试液变红,碱性溶液的pH大于7,加入稀硫酸后则稀硫酸能与氢氧化钠反应而使碱性消失,酚酞在酸性或中性溶液中为无色,故会看到溶液由红色逐渐变为无色,碱性逐渐消失,则溶液的pH减小;
(2)酸性溶液越稀,则pH越大,可以加水使pH增大,也可以加入碱性物质与酸反应的方法.
故答案为:(1)没加稀硫酸之前溶液为红色,当加入稀硫酸后,溶液溶液颜色逐渐变浅直至变为无色;减小;
(2)加水或加入氢氧化钠溶液.
(2)酸性溶液越稀,则pH越大,可以加水使pH增大,也可以加入碱性物质与酸反应的方法.
故答案为:(1)没加稀硫酸之前溶液为红色,当加入稀硫酸后,溶液溶液颜色逐渐变浅直至变为无色;减小;
(2)加水或加入氢氧化钠溶液.
点评:本题考查酸碱混合的判断,题目难度不大,溶液酸碱性以及pH的大小取决于溶液中H+与OH-离子的浓度大小关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、Cl-的质子数比电子数多1 |
| B、NaCl由Cl-和Na+构成 |
| C、原子都由质子、中子、电子构成 |
| D、保持水的化学性质的最小粒子是H和O |


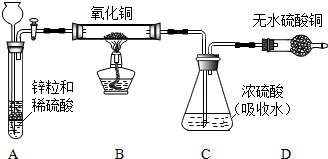
 化学兴趣小组的同学探究铁的化学性质时进行了如下实验.
化学兴趣小组的同学探究铁的化学性质时进行了如下实验.