题目内容
为测定变质前Ca(OH)2样品[含Ca(OH)2和CaCO3]中Ca(OH)2的质量,张南同学取部分变质的样品12.4g,向其中加入溶质质量分数为7.3%稀盐酸,至不再产生气泡为止,产生气体2.2g,消耗稀盐酸质量为150g.则未变质前Ca(OH)2的质量为( )
| A、7.4g | B、11.1g |
| C、3.7g | D、14.8g |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据氢氧化钙和盐酸反应生成氯化钙和水,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,所以未变质前Ca(OH)2与变质后Ca(OH)2中消耗盐酸的质量相等,利用盐酸中氯化氢的质量求出氢氧化钙的质量即可.
解答:解:由CO2+Ca(OH)2═CaCO3↓+H2O、CaCO3+2HCl═CaCl2+H2O+CO2↑、Ca(OH)2+2HCl═CaCl2+2H2O可知,
参加反应的盐酸和氢氧化钙的关系为:Ca(OH)2~2HCl
设未变质前Ca(OH)2的质量为x.
Ca(OH)2~2HCl
74 73
x 150g×7.3%
=
x=11.1g
答:未变质前Ca(OH)2的质量为11.1g.
故答案为:B.
参加反应的盐酸和氢氧化钙的关系为:Ca(OH)2~2HCl
设未变质前Ca(OH)2的质量为x.
Ca(OH)2~2HCl
74 73
x 150g×7.3%
| 74 |
| x |
| 73 |
| 150g×7.3% |
x=11.1g
答:未变质前Ca(OH)2的质量为11.1g.
故答案为:B.
点评:此题是对化学式和化学反应问题的考查,解题的关键是利用质量守恒定律对反应前后钙元素的质量不变的分析.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
下列物质溶于水时发生了化学变化的是( )
| A、二氧化碳 | B、冰 |
| C、味精 | D、氯化钠 |
阿司匹林(化学式为C9H8O4)是一种常见的解热镇痛药,下列说法错误的是( )
| A、阿司匹林中含有21个原子 |
| B、阿司匹林属于有机化合物 |
| C、阿司匹林由碳、氢、氧三种元素组成 |
| D、阿司匹林的相对分子质量为180 |
如图是用海水提取粗盐的大致过程.下列说法错误的是( )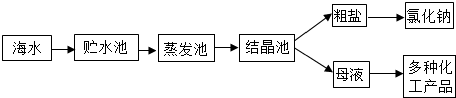

| A、海水进入贮水池,海水的成分基本不变 |
| B、析出晶体后的母液是氯化钠的不饱和溶液 |
| C、在蒸发池中,海水中水的质量逐渐减少 |
| D、在蒸发池中,海水中氯化钠的质量分数逐渐增大 |
化学改变世界的途径是使物质发生化学变化.下列变化中属于化学变化的是( )
| A、石油分馏出汽油、煤油、柴油 |
| B、利用膜法从海水中获得淡水 |
| C、铁矿石冶炼成铁 |
| D、工业上从空气中分离出氧气 |