题目内容
14.通过学习,我们已经认识了食盐的主要成分氯化钠的构成粒子,其符号为Na+和Cl-;某同学在配制5%的氯化钠溶液时,若量取水时仰视量筒读数,则会导致所配制溶液的溶质质量分数偏小(填“偏大”、“偏小”或“不变”);在氯化钠溶液中滴加硝酸银溶液,产生白色沉淀,反应的化学方程式为NaCl+AgNO3═NaNO3+AgCl↓.分析 构成氯化钠的微粒是钠离子和氯离子,写出其离子符号即可.
根据用量筒量取水时,仰视液面,读数比实际液体体积小,进行分析解答.
氯化钠溶液与硝酸银溶液反应生成氯化银沉淀和硝酸钠,写出反应的化学方程式即可.
解答 解:构成氯化钠的微粒是钠离子和氯离子,其离子符号为Na+和Cl-.
用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
氯化钠溶液与硝酸银溶液反应生成氯化银沉淀和硝酸钠,反应的化学方程式为:NaCl+AgNO3═NaNO3+AgCl↓.
故答案为:Na+和Cl-;偏小;NaCl+AgNO3═NaNO3+AgCl↓.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的注意事项、物质的微观构成、盐的化学性质是正确解答本题的关键.

练习册系列答案
相关题目
6.常见原子团及化合价
| 原子团名称 | 原子团符号 | 化合价 |
| 硫酸根 | ||
| 碳酸根 | ||
| 氢氧根 | ||
| 硝酸根 | ||
| 铵根 |
3.在pH=7的某无色溶液中,能大量共存的是( )
| A. | Na+,Fe2+,NO3-,Cl- | B. | Na+,K+,NO3-,CO32- | ||
| C. | Ba2+,K+,SO42-,Cl- | D. | NH4+,K+,OH-,SO42- |
20.化学时刻影响着我们的生活,它在工农业生产和日常生活中起到了非常重要的作用.下列说法中正确的是( )
| A. | 为提高牛奶的含氮量,可向牛奶中添加三聚氰胺 | |
| B. | 熟石灰可以改良酸性土壤,但不能和硫酸铵混合使用 | |
| C. | 纤维素无法被人体吸收,所以食物中的纤维素对人体毫无意义 | |
| D. | 木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关 |

 表示氢原子,
表示氢原子, 表示氧原子)
表示氧原子)

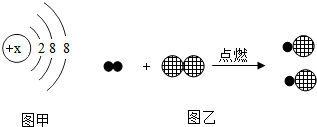 图甲是某粒子A-的结构示意图,图乙是相对分子质量最小的单质与A的单质反应的微观模拟图.回答:
图甲是某粒子A-的结构示意图,图乙是相对分子质量最小的单质与A的单质反应的微观模拟图.回答: