题目内容
4.小煜通过学习知道:Na2CO3、NaHCO3均能与盐酸反应,Na2CO3溶液还会与石灰水反应.【产生疑问】NaHCO3溶液也能与石灰水反应吗?如果能反应,生成物可能是什么?
【进行实验】小煜将NaHCO3溶液与石灰水混合,结果产生了白色沉淀.已知Ca(HCO3)2能溶于水,碳酸氢盐在碱溶液中会生成碳酸盐.此白色沉淀是碳酸钙,证明NaHCO3溶液与Ca(OH)2 溶液也能发生反应.为了进一步了解生成的含钠化合物有什么,继续探究:
【作出猜想】①只有NaOH;②Na2CO3和NaOH;③Na2CO3
【实验设计】
步骤1:取少量上述实验后的上层清液于试管中,再滴加足量的CaCl2 溶液(中性),观察到产生白色沉淀,由此可知生成的含钠化合物中一定含有碳酸钠;
步骤2:将步骤1中后应后的混合物过滤,往滤液中先滴加几滴无色酚酞溶液,再滴加足量的稀盐酸,观察到溶液颜色变化情况为溶液由无色变红色,又由红色变为无色,整个实验过程中无气泡产生,由此可知猜想①成立.
【拓展提高】若步骤1中未出现白色沉淀,则此时NaHCO3溶液与Ca(OH)2 溶液反应的化学方程式为Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O.
分析 【进行实验】根据碳酸氢盐在碱溶液中会生成碳酸盐可以判断白色沉淀
【作出猜想】根据题干结合所学知识做出合理的猜想
【实验设计】根据所做实验结合钙离子能够和碳酸根离子生成白色沉淀,酚酞遇碱变红色等知识点可以完成解答
【拓展提高】以为氯化钙可以和碳酸钠反应生成白色沉淀碳酸钙,如果不生成白色沉淀,则说明没生成碳酸钠,则可以据此写出化学方程式
解答 解:【进行实验】
根据碳酸氢盐在碱溶液中会生成碳酸盐可以判断白色沉淀,故本题答案为:碳酸钙;
【作出猜想】
根据题干结合所学知识做出合理的猜想,故本题答案为:Na2CO3;
【实验设计】
实验1,加入氯化钙产生白色沉淀,能够和氯化钙反应生成沉淀的只有碳酸钠,故本题答案为:碳酸钠;
实验2,若猜想2正确说明有氢氧化钠,所以在滤液中含有氢氧化钠,当加入酚酞试液后滤液会变红,再滴加足量的稀盐酸,会把氢氧化钠中和掉,故红色又会消失,故本题的答案为:溶液由无色变红色,又由红色变为无色;①;
【拓展提高】
若步骤1中没有产生沉淀,则说明碳酸氢钠和氢氧化钙没有生成碳酸钠而是生成了碳酸钙,所以可以写出碳酸氢钠和氢氧化钙反应的化学方程式.故本题答案为:Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O.
点评 熟练掌握碳酸钠、碳酸氢钠和氢氧化钙的化学性质,知道酚酞遇碱的溶液会变红,能够根据题给的信息来完成化学方程式:Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列粒子结构示意图中,表示阳离子的是( )
| A. |  | B. | 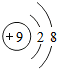 | C. | 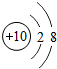 | D. |  |
12.将下列物质中所含杂质除去,所选除杂试剂正确的是( )
| 序号 | 物质 | 所含杂质 | 除杂试剂 |
| A | O2 | CO2 | NaOH溶液 |
| B | CaCO3 | CaCl2 | 稀盐酸 |
| C | 盐酸 | 稀硫酸 | BaCl2溶液 |
| D | KNO3溶液 | KOH | FeCl3溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.类推是学习化学的重要方法之一,但盲目类推又可能得出错误结论.下列类推正确的是( )
| A. | 原子和分子均是微观粒子,原子在化学变化中不能再分,则分子在化学变化中也不能再分 | |
| B. | 锌和铜均是金属,锌能与稀硫酸反应放出氢气,则铜也能与稀硫酸反应放出氢气 | |
| C. | 金刚石和石墨均是碳的单质,金刚石十分坚硬,则石墨也十分坚硬 | |
| D. | H2SO4与HCl均是酸,H2SO4在水溶液中能电离出H+,则HCl在水溶液中也能电离出H+ |
16.下列变化中属于物理变化的是( )
| A. | 镁带燃烧 | B. | 植物的光合作用 | C. | 木材做成课桌 | D. | 火药爆炸 |
13. 有关电解水实验(如图)的下列叙述,错误的是( )
有关电解水实验(如图)的下列叙述,错误的是( )
 有关电解水实验(如图)的下列叙述,错误的是( )
有关电解水实验(如图)的下列叙述,错误的是( )| A. | 试管甲中的气体能燃烧 | |
| B. | 试管乙中的气体是氧气 | |
| C. | 该实验证明水由氢元素和氧元素组成 | |
| D. | 该实验证明水由氢气和氧气组成 |