题目内容
10.根据如图所示装置图,回答有关问题: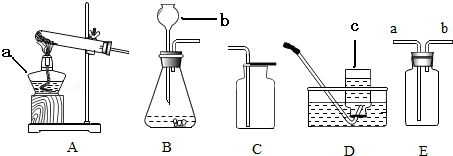
(1)指出图中标号仪器的名称:a酒精灯、b长颈漏斗、c集气瓶
(2)写出实验室用H2O2制了氧气的化学方式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰起催化作用.
(3)若用氯酸钾制取氧气,可选用的发生装置是A(填字母),反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该反应为分解反应.
(4)指出装置B中的错误长颈漏斗没有伸入到液面以下.
(5)实验室除用装置C和D收集氧气外,还可用E装置收集氧气.若将E装置装满水来收集该气体,应从b(填“a”或“b”)端通入气体.
分析 (1)按照图示填写仪器名称;
(2)根据反应物、生成物及质量守恒定律分析;催化剂在化学反应中起催化作用,能改变化学反应速率;
(3)根据反应物的状态和反应条件分析;根据化学方程式的书写方法及反应类型的特征分析;
(4)根据实验装置进行分析;
(5)根据气体的性质和装置的特点分析;
解答 解:(1)仪器名称为a是酒精灯;b是长颈漏斗;c是集气瓶.故答案为:酒精灯;长颈漏斗;集气瓶;
(2)二氧化锰在这个反应中是催化剂,所以二氧化锰所起的作用是催化作用,能改变物质的化学反应速率,其反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.故答案为:催化作用;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)反应物是氯酸钾,需要加热,故发生装置应选A;生成物是氯化钾、氧气,其反应的化学方程式:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该反应符合一变多的特征,属于分解反应;故答案为:A;2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;分解;
(4)装置B中的错误是长颈漏斗没有伸入到液面以下,会造成生成的气体经过长颈漏斗跑掉;故答案为:长颈漏斗没有伸入到液面以下;
(5)因为氧气不溶于水,可用排水法收集,若用E装置收集氧气.应该遵循短进的原则,让水由长导管排出;故答案为:b;
点评 本题综合考查气体实验室制取原理和装置的选择,同时考查催化剂和催化作用.

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
15.下列微粒中.其质子数和电子数跟OH-离子都相同的是( )
| A. | Na+ | B. | O2- | C. | F- | D. | Mg2+ |
15.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量盐酸,塞上带导管的单孔塞,把导管插入另一试管里的石灰水中. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 品红溶液褪色 |
2.下列基本实验操作正确的是( )
| A. |  检查气密性 | B. |  测量溶液的pH | ||
| C. |  取固体药品 | D. |  熄灭酒精灯 |
19.用托盘天平秤8.5g石灰石,把砝码放在了左盘,石灰石放在了右盘(1g以下用游码),则称量结果( )
| A. | 8.5克 | B. | 大于8.5克 | C. | 小于8.5克 | D. | 无法称量 |
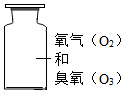
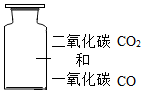

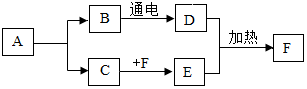
 已知A、B、C、D、E是初中化学常见的五种物质,均含有同一种元素,其中,只有A为单质,B个C含有的元素完全相同,D与其他四种物质的类别不同,E是一种重要建筑材料的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已略去),则A→C、B→E反应的化学方程式分别为2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO、CO2+Ca(OH)2=CaCO3↓+H2O;举例说明在日常生活中,对可能有物质C生成的情况,我们应怎样处理用煤火取暖时,一定要装烟囱,并且注意通风,防止一氧化碳中毒.
已知A、B、C、D、E是初中化学常见的五种物质,均含有同一种元素,其中,只有A为单质,B个C含有的元素完全相同,D与其他四种物质的类别不同,E是一种重要建筑材料的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已略去),则A→C、B→E反应的化学方程式分别为2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO、CO2+Ca(OH)2=CaCO3↓+H2O;举例说明在日常生活中,对可能有物质C生成的情况,我们应怎样处理用煤火取暖时,一定要装烟囱,并且注意通风,防止一氧化碳中毒.