题目内容
3.下列有关盐酸、稀硫酸的叙述正确的是( )| A. | 打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾 | |
| B. | 稀盐酸和稀硫酸都可以用于实验室制二氧化碳 | |
| C. | 浓盐酸、浓硫酸都可用来干燥氧气 | |
| D. | 稀盐酸和稀硫酸都可用于除铁锈 |
分析 根据已有的酸的性质和用途进行分析解答即可.
解答 解:A、浓硫酸不具有挥发性,不会形成白雾的现象,错误;
B、稀硫酸与石灰石反应生成的硫酸钙覆盖在石灰石的表面,阻止反应的进行,错误;
C、浓盐酸不具有吸水性,不能用于干燥氧气,错误;
D、稀盐酸和稀硫酸都能与金属氧化物反应,可以用于清除铁锈,正确;
故选D.
点评 本题考查的是常见的酸的性质和用途,完成此题,可以依据已有的知识进行.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
13.用化学符号表示:
| (1) | (2) | (3) | (4) | |
| 化学符号 | O | NH4+ | nOH- | $\stackrel{+3}{Fe}$2O3 |
| 表示意义 | 湖水中含量最高的元素 | 硝酸铵中的阳离子 | n个氢氧根离子 | 标出氧化铁中铁元素的化合价 |
11.科学家发现,水在一157℃超低温、正常压力或真空条件下仍呈液态,比蜂蜜还粘稠,称为“高密度液态水”.下列关于这种“高密度液态水”的说法正确的是( )
| A. | 化学性质与水不同 | |
| B. | 分子不再运动 | |
| C. | 氢、氧两种原子的个数比为2:1 | |
| D. | 分子间的间隔比普通的液态水(0一100℃)的大 |
13. 小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
【第一组实验】检验该双氧水是否失效.
(1)实验过程
①在试管中加入5mL 的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如图装置进行操作,带火星的木条复燃,水槽中冰水所起让水蒸汽冷凝的作用.
(2)实验结论:双氧水没有失效.
【第二组实验探究】:氧化铜(CuO)能否催化“双氧水”分解
[猜想]Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
[实验]用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验:
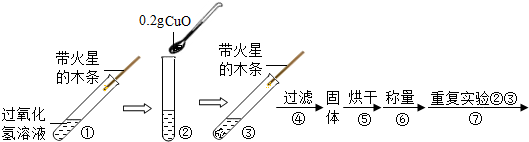
(3)完成下表:
(4)步骤③结束后,用手接触试管底部,感觉烫手.说明“双氧水”分解的化学反应放热(选填“放热”或“吸热”).
(5)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒.
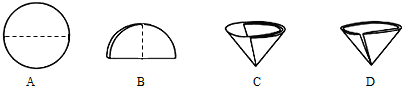
(6)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D(填序号).
(7)步骤⑦的目的检验氧化铜化学性质是否改变.
(8)过氧化氢能被CuO催化分解放出O2的反应表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
 小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.【第一组实验】检验该双氧水是否失效.
(1)实验过程
①在试管中加入5mL 的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如图装置进行操作,带火星的木条复燃,水槽中冰水所起让水蒸汽冷凝的作用.
(2)实验结论:双氧水没有失效.
【第二组实验探究】:氧化铜(CuO)能否催化“双氧水”分解
[猜想]Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
[实验]用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验:

(3)完成下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡冒出, 带火星的木条复燃 | 仍为0.2g (氧化铜质量不变) | 溶液中有气泡放出, 使带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立 |
(5)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒.
(6)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D(填序号).

(7)步骤⑦的目的检验氧化铜化学性质是否改变.
(8)过氧化氢能被CuO催化分解放出O2的反应表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.