题目内容
某同学将镁和金属X的混合物共2.4 g加入足量的稀硫酸,充分反应后得到0.22 gH2,则金属X可能是( )
A.Al B.Zn C.Fe D.Cu
A
【 解析】设该金属全部是镁,2.4 g镁与硫酸反应产生氢气的质量为x,则:
解析】设该金属全部是镁,2.4 g镁与硫酸反应产生氢气的质量为x,则:
Mg + H2SO4===MgSO4 + H2↑
24 2
2.4 g x
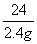 =
=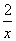
解得x=0.2 g,因为收集到0.2 2 g H2,所以另一种金属产生氢气的质量必须比同质量的镁产生氢气质量多,铝产生的氢气比相同质量的镁产生氢气多,铁、锌产生的氢气比相同质量的镁产生氢气少,而铜不与酸反应,所以可能是铝。
2 g H2,所以另一种金属产生氢气的质量必须比同质量的镁产生氢气质量多,铝产生的氢气比相同质量的镁产生氢气多,铁、锌产生的氢气比相同质量的镁产生氢气少,而铜不与酸反应,所以可能是铝。

练习册系列答案
相关题目

 a2CO3受热不易分解,2NaHCO3
a2CO3受热不易分解,2NaHCO3 Na2CO3+CO2↑+H2O。某纯碱样品中混有少量的碳酸氢钠,为了测定样品的纯度,华雪同学做了如下实验:准确称取样品10.0 g放入试管中,加热充分反应至无气体放出,共
Na2CO3+CO2↑+H2O。某纯碱样品中混有少量的碳酸氢钠,为了测定样品的纯度,华雪同学做了如下实验:准确称取样品10.0 g放入试管中,加热充分反应至无气体放出,共 单位负电荷,因此碳原子
单位负电荷,因此碳原子 物质的克数是 ( )
物质的克数是 ( )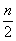 -e B.m+2n-e
-e B.m+2n-e