题目内容
(2010?东城区二模)常用化肥硫酸铵分解的化学方程式为:3(NH4)2SO4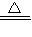 4NH3↑+3X↑+N2↑+6H2O,则X中各元素的化合价分别是( )
4NH3↑+3X↑+N2↑+6H2O,则X中各元素的化合价分别是( )
【答案】分析:先根据化学方程式为3(NH4)2SO4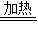 4NH3↑+3X↑+N2↑+6H2O,利用质量守恒定律来推断X的化学式,然后利用化学式和化合价的计算原则来计算各元素的化合价.
4NH3↑+3X↑+N2↑+6H2O,利用质量守恒定律来推断X的化学式,然后利用化学式和化合价的计算原则来计算各元素的化合价.
解答:解:在反应3(NH4)2SO4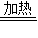 4NH3↑+3X↑+N2↑+6H2O中,
4NH3↑+3X↑+N2↑+6H2O中,
根据质量守恒定律可知,反应前后元素的种类、原子个数不变,
N、H元素的原子前后相等,S、O原子的个数不等,
反应前共3个S原子,12个O原子,
则反应后X中有3个S原子,反应后现有6个O原子,则X中共有6个O原子,
又X的化学计量数为3,则X的化学式为SO2;
在SO2中,根据氧化物可知O元素的化合价为-2价,
根据化合物中正负化合价的代数和为0,设S元素的化合价为x,
则x+(-2)×2=0
解得x=+4
即SO2中的元素化合价分别为+4,-2;
故选B.
点评:本题考查元素化合价的计算,考查学生分析解决问题的能力,学生应明确解答的思路是先利用化学方程式推断化学式,再利用化学式计算化合价来解答.
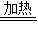 4NH3↑+3X↑+N2↑+6H2O,利用质量守恒定律来推断X的化学式,然后利用化学式和化合价的计算原则来计算各元素的化合价.
4NH3↑+3X↑+N2↑+6H2O,利用质量守恒定律来推断X的化学式,然后利用化学式和化合价的计算原则来计算各元素的化合价.解答:解:在反应3(NH4)2SO4
 4NH3↑+3X↑+N2↑+6H2O中,
4NH3↑+3X↑+N2↑+6H2O中,根据质量守恒定律可知,反应前后元素的种类、原子个数不变,
N、H元素的原子前后相等,S、O原子的个数不等,
反应前共3个S原子,12个O原子,
则反应后X中有3个S原子,反应后现有6个O原子,则X中共有6个O原子,
又X的化学计量数为3,则X的化学式为SO2;
在SO2中,根据氧化物可知O元素的化合价为-2价,
根据化合物中正负化合价的代数和为0,设S元素的化合价为x,
则x+(-2)×2=0
解得x=+4
即SO2中的元素化合价分别为+4,-2;
故选B.
点评:本题考查元素化合价的计算,考查学生分析解决问题的能力,学生应明确解答的思路是先利用化学方程式推断化学式,再利用化学式计算化合价来解答.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
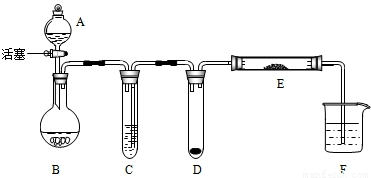
(2010?东城区二模)某班同学到实验室进行气体的制取实验,实验桌上摆放了下列仪器可供选用(铁架台省略).

请回答下列问题:
(1)仪器a的名称是.
(2)组合一套制备并收集CO2的实验装置,应选用的仪器是(填字母序号).
(3)如果用制取二氧化碳的装置来制取氧气,则反应的化学方程式是.
(4)阅读以下资料并回答:
制取氯气(填“可以”或“不可以”)采用制取二氧化碳气体的发生装置,收集氯气可以选用的仪器是(填字母序号).

请回答下列问题:
(1)仪器a的名称是.
(2)组合一套制备并收集CO2的实验装置,应选用的仪器是(填字母序号).
(3)如果用制取二氧化碳的装置来制取氧气,则反应的化学方程式是.
(4)阅读以下资料并回答:
| 物质 | 制取气体的药品 | 制取气体的反应条件 | 气体的物理性质 |
| 氯气 | 固体二氧化锰、液体浓盐酸 | 需要加热 | 密度比空气大、能溶于水 |
 6CO2+6H2O下列分析错误的是( )
6CO2+6H2O下列分析错误的是( )

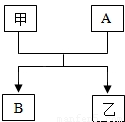 (2010?东城区二模)已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示.
(2010?东城区二模)已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示.