题目内容
5.除去下列物质中的少量杂质(括号内是杂质),所用试剂及方法均正确的是( )| A. | 二氧化碳(一氧化碳)--通过足量的氢氧化钠溶液、干燥 | |
| B. | 硫酸亚铁溶液(硫酸铜)--加过量的锌粉、过滤 | |
| C. | 氢氧化钠(碳酸钠)--加适量的稀盐酸、蒸发 | |
| D. | 氮气(氧气)--通过灼热的铜网 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、硫酸亚铁溶液和硫酸铜溶液均能与锌粉反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、氢氧化钠、碳酸钠均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
15.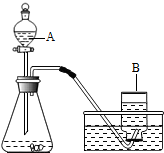 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前,小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是检查装置的气密性.
(2)小红同学通过互联网得知:CuSO4 溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.动物脏器中含有过氧化氢酶,能催化过氧化氢分解,过氧化氢酶是蛋白质(选填糖类、蛋白质、脂肪或维生素),实验证明,CuSO4 溶液能催化过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了如下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是过氧化氢溶液中含有水.
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
③如果要确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后质量和化学性质没有改变.
 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前,小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是检查装置的气密性.
(2)小红同学通过互联网得知:CuSO4 溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.动物脏器中含有过氧化氢酶,能催化过氧化氢分解,过氧化氢酶是蛋白质(选填糖类、蛋白质、脂肪或维生素),实验证明,CuSO4 溶液能催化过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了如下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是过氧化氢溶液中含有水.
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是Cu2+ |
| b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴氯化铜溶液 | 溶液中有大量产泡放出 |
20.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 氢氧化钙 熟石灰 CaO | B. | 汞 水银 Hg | ||
| C. | 二氧化碳 冰CO2 | D. | 碳酸钠 烧碱 Na2CO3 |
10.以下自然资源的利用过程中,发生了化学变化的是( )
| A. | 海水晒盐 | B. | 风力发电 | C. | 铁矿石炼铁 | D. | 石油分馏 |
17.下列实验操作中,不正确的是( )
| A. | 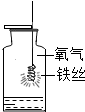 铁丝在氧气中燃烧 | B. | 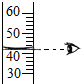 读取液体的体积 | ||
| C. | 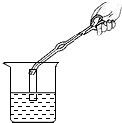 测溶液的pH | D. | 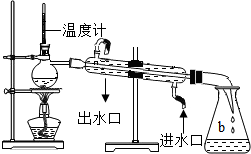 制取蒸馏水 |
14.在一定条件下,下列转化不能由一步反应实现的是( )
| A. | H2O→CO2 | B. | (NH4)2SO4→NH3 | C. | Cu→Cu(NO3)2 | D. | MgO→MgCl2 |
15.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物.与较粗的大气颗粒物相比,PM2.5粒径小,富含大量的有毒、有害物质且在大气中的停留时间长、输送距离远,因而对人体健康和大气环境质量的影响更大.下列关于PM2.5的说法中,正确的是( )
| A. | PM2.5主要是由于化石燃料的大量燃烧引起的,所以,为了降低空气中PM2.5的含量,我们应该马上停止使用化石燃料 | |
| B. | 鼻腔内的绒毛对空气中较粗的颗粒物具有一定的阻挡作用,这属于特异性免疫 | |
| C. | PM2.5主要是通过消化道进入人体内部的 | |
| D. | 减少PM2.5对保护环境,维持生态系统的稳定性将起到重要作用 |
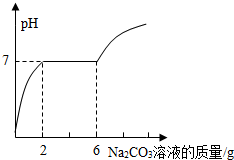 某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶解加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶解加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究. 目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源,因此,开发利用新能源就显得格外重要.
目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源,因此,开发利用新能源就显得格外重要.