题目内容
15.某同学为了研究酒精的性质,做了如下探究,请你把他的探究情况完成.(1)通过观察酒精灯内的酒精,酒精的颜色是无色液体;
(2)闻闻它的气味,酒精有特殊的气味;
(3)用滴管吸取一些酒精滴入盛有少量水的试管中,可见酒精溶(填“溶”或“不溶”)于水;
(4)用火柴点燃酒精灯,然后把干燥的冷烧杯罩在酒精灯的火焰上方,发现烧杯内壁有水雾出现,把烧杯倒立过来立即注入少量澄清石灰水,振荡后发现石灰水变浑浊,通过这两个现象说明酒精燃烧时生成水和二氧化碳,该反应的文字表达式为酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水.
分析 根据已有的酒精的物理性质和燃烧的现象进行分析解答即可.
解答 解:(1)酒精是无色的液体,故填:无,液;
(2)酒精有特殊的香味,故填:特殊;
(3)酒精是易溶于水的物质,故填:溶;
(4)用火柴点燃酒精灯,然后把干燥的冷烧杯罩在酒精灯的火焰上方,发现烧杯内壁有水雾出现,把烧杯倒立过来立即注入少量澄清石灰水,振荡后发现石灰水变浑浊,说明酒精燃烧生成了水和二氧化碳,故填:水珠,变浑浊,水,二氧化碳,酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水.
点评 本题考查的是酒精的有关性质和燃烧产物的推断,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.化学兴趣小组对“影响金属与盐酸反应剧烈程度的因素”进行了探索.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
c、…
【活动探究1】为探究猜想a,分别在两支试管中放入相同质量的锌片和铁片(所用金属均已用砂纸打磨),然后分别加入相同尝试和质量的稀盐酸,
(1)观察到放锌片的试管中立即产生大量气泡,发生反应的化学方程式是Zn+2HCl═ZnCl2+H2↑.
(2)放铁片的试管中只产生少量气泡,溶液由无色变为浅绿色.
(3)从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
(4)得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属的活动性越强,与相同的盐酸反应越剧烈.
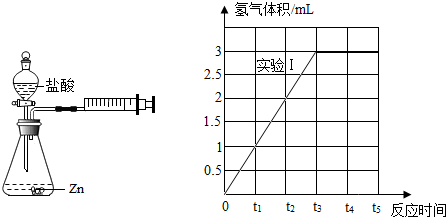
【活动探究2】为探究猜想b,设计如图的装置进行实验,其中注射器用于测量产生氢气的体积.
所用药品,实验数据如表(盐酸足量):
(5)请在坐标图中画出实验编号Ⅱ产生氢气与时间的关系图.
(6)得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是相同条件下,盐酸的浓度越大,金属与盐酸反应越快(“块”或“慢”).
(7)通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响温度(写一条即可).
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
c、…
【活动探究1】为探究猜想a,分别在两支试管中放入相同质量的锌片和铁片(所用金属均已用砂纸打磨),然后分别加入相同尝试和质量的稀盐酸,
(1)观察到放锌片的试管中立即产生大量气泡,发生反应的化学方程式是Zn+2HCl═ZnCl2+H2↑.
(2)放铁片的试管中只产生少量气泡,溶液由无色变为浅绿色.
(3)从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
(4)得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属的活动性越强,与相同的盐酸反应越剧烈.
【活动探究2】为探究猜想b,设计如图的装置进行实验,其中注射器用于测量产生氢气的体积.
所用药品,实验数据如表(盐酸足量):
| 实验编号 | 选用金属(质量形状相同) | 盐酸浓度(相同体积) | 产生氢气的体积/mL | |||||
| 0 | t1 | t2 | t3 | t4 | t5 | |||
| Ⅰ | 锌片 | 6% | 0 | 1 | 2 | 3 | 3 | 3 |
| Ⅱ | 锌片 | 3% | 0 | 0.6 | 1.2 | 1.8 | 2.4 | 3 |
(6)得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是相同条件下,盐酸的浓度越大,金属与盐酸反应越快(“块”或“慢”).
(7)通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响温度(写一条即可).

3.氢氧化铝[Al(OH)3]受热易分解,产生水并吸收热量,故可用作阻燃剂;能与盐酸、NaOH溶液反应,是药物“复方胃舒平”的主要成分之一.实验室制备Al(OH)3方法为:Al2(SO4)3+6NH3•H2O═2Al(OH)3↓+3(NH4)2SO4,通常不选用NaOH.下列判断不正确的是( )
| A. | 氢氧化铝的化学性质稳定 | |
| B. | 复方胃舒平可用于治疗胃酸过多症 | |
| C. | 氢氧化铝可灭火的原因之一是降低了可燃物的着火点 | |
| D. | 实验室不用NaOH溶液制备Al(OH)3,因为NaOH会与Al(OH)3反应 |
10.某同学在实验室配制50g6%的氯化钠溶液,下图所示的部分操作其中错误的是( )
| A. | 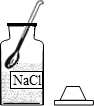 取一定量的NaCl | B. | 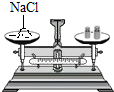 称取3gNaCl | C. |  量取47mL水 | D. | 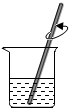 溶解 溶解 |
4.净化水的以下操作,其中净化程度最高的是( )
| A. | 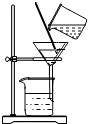 过滤 | B. |  蒸发 | ||
| C. | 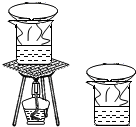 蒸馏 | D. |  吸附 |

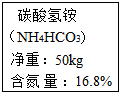 回答下列问题:
回答下列问题: