题目内容
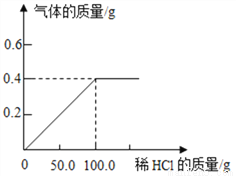
黄铜中锌的含量影响到它的性能,含锌量大于46%~50%的黄铜因性能硬脆,不能进行压力加工,为了测定某黄铜中锌的质量分数,取30.0 g黄铜(铜锌合金)样品,向其中逐渐加入稀HCl,产生气体质量与加入稀HCl质量的关系如图所示。请计算(计算结果精确到0.1%):(锌与盐酸反应的化学方程式为Zn+2HCl=ZnCl2+H2↑)
(1)样品中Zn的质量分数为____________。
(2)将反应后溶液蒸发44.8g的水后,溶液中溶质的质量分数为____________。
43.3% 40% 【解析】本题考查了溶质质量分数与化学方程式相结合的计算。 由图可以看出生成氢气的质量为0. 4g; 参加反应的锌的质量为x,反应后生成氯化锌质量为y。 Zn+2HCl=ZnCl2+H2↑ 65 136 2 x y 0.4g x=13g y=27.2g (1)样品中Zn的质量分数=×100%= 43.3%; (2) 溶液...
练习册系列答案
相关题目