题目内容
17.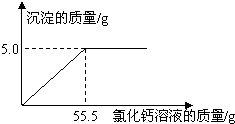 用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品5.5g,充分溶解于44g水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如右图所示.求:
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品5.5g,充分溶解于44g水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如右图所示.求:(1)该纯碱样品中碳酸钠的质量分数.(精确到0.1%)
(2)求恰好完全反应时溶液中溶质质量分数.
分析 (1)计算该纯碱样品中碳酸钠的质量分数,先根据化学方程式求出样品中碳酸钠的质量,再利用质量分数公式计算即可.
(2)计算恰好完全反应时溶液(氯化钠溶液)中溶质质量分数,先根据化学方程式求出溶质的质量,再根据溶质质量分数的计算公式进行计算即可.
解答 解:设纯碱样品中含有碳酸钠的质量为x,充分反应后生成氯化钠的质量为y.
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100 117
x 5.0g y
$\frac{106}{x}=\frac{100}{5g}=\frac{117}{y}$
x=5.3g y=5.85g
(1)纯碱样品中含有碳酸钠的质量分数=$\frac{5.3g}{5.5g}×100%$=96.4%;
(2)恰好反应时,溶液中氯化钠的质量分数=$\frac{5.5g-5.3g+5.85g}{5.5g+44g+55.5g-5g}×100%$=6.05%
答:(1)纯碱样品中含有碳酸钠的质量分数为96.4%;
(2)恰好反应时,溶液中溶质,及氯化钠的质量分数6.05%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题意题意、图表信息等各种信息,根据图象确定沉淀的质量是正确解答本题的前提和关键.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案
相关题目
7.化学与生活密切相关,下列说法不正确的是( )
| A. | 糖类和蛋白质都能为人体提供能量 | |
| B. | 新鲜蔬菜、水果中富含维生素 | |
| C. | 人体缺锌易患贫血病 | |
| D. | 磷肥可以促进作物生长,增强植物的抗寒、抗旱能力 |
9.下列物质的分类正确的是( )
| A. | 混合物:空气、天然气、水蒸气 | B. | 能置换出酸中氢的金属:铝、铁、汞 | ||
| C. | 氧化物:水、酒精、干冰 | D. | 磷单质:红磷、白磷 |